2010.05.22 Saturday
 |
|
不育症診療の最近の進歩
【参考文献】
「産婦人科治療」 (永井書店) Vol. 83, 2001 p.41-44
生殖医学の進歩と生殖医療の限界
不育症診療の最近の進歩
Recent progress in the management of recurrent pregnancy losses
東海大学医学部母子生育学系産婦人科学部門
牧野恒久教授 杉 俊隆講師
--------------------------------------------------------------------------------
Summary
不育症の分野は最近目覚ましい進歩を遂げている。その結果、以前は原因不明であった難治性習慣流産の患者の多くの診断、治療が可能となりつつある。特に、抗リン脂質抗体症候群を始めとした生殖免疫学と血液凝固学にまたがる分野が脚光を浴び、血液、リウマチ、免疫、生殖など多くの分野の専門家が学際的に研究を進め、今日の不育症の進歩があると言える。本稿では最近の不育症管理の新しい概念について解説する。
はじめに
子宮は今だにブラックボックスであり、着床から妊娠、分娩に至るまでutero-placental unitで何が起きているのか不明の点が多い。それにもかかわらず不育症の分野は最近10年で大いなる発展を遂げてきた。その内容は、生殖免疫、血液凝固学の進歩に依るところが多く、高度に専門化しつつある。本稿では、不育症について概説し、さらには最先端の知見なども併せて紹介したい。
不育症、習慣流産とは
"不育症"とは、厳密な定義をもつ医学用語ではない。強いて定義付ければ、成立した妊娠を完遂できず、健康な生児に恵まれない症例を指すものといえる。一般的には習慣流産を指すことが多いが、同義ではない。習慣流産とは、3回以上流産を繰り返すことであり、時期は妊娠22週未満に限定される。しかしながら、不育症と言った場合は妊娠中期以降の子宮内胎児死亡や反復流産(流産回数2回)も含まれ得る。不育症に相当する英語としては、recurrent fetal lossという表現をしばしば目にするが、fetus(胎児)という名称は妊娠10週以後に限定され、それ以前のembryo(胎芽)が含まれないので、recurrent pregnancy lossが適当であると思われる。
一回の独立した流産の頻度は統計上約15-20%であり、決して珍しくない。その約60-70%以上は胎児に染色体異常があると報告されている。また、受精卵の約40%に染色体異常があり、それが出生時には0.6%に減少すると報告されており、もし流産という自然淘汰がおこらなければ、出生した児の40%が染色体異常をもつことになる1)。したがってある意味では、流産の多くは病的ではなく、それを止めることもできないし、止める必要も無いということになる。一回や二回の流産既往があっても、それが直ちに病的であり、不育症であるということにはならない。ちなみに、一回の独立した妊娠の流産の頻度を20%と仮定すると、2回反復流産率は0.2×0.2=0.04で4%、3回習慣流産率は0.04×0.2=0.008で0.8%となる。したがって、2回反復流産の場合は病的原因をもたず、不育症とは言えない場合も多いが、3回以上自然流産を繰り返した習慣流産の場合は自然淘汰という考えでは確率的に説明できず、不育症の原因を検索する事になる。
1..内分泌異常と不育症に関する最近の概念
不育症の患者に対して内分泌系の検査を施行し、何か異常が見い出されればそれが原因であると診断して治療することは非常に基本的な事であると一般には考えられている。しかしながら、意外にも内分泌異常が本当に流産の原因になり得るのか証明されていない事が多い。以下に、代表的内分泌異常について不育症との関係を概説する。
1)黄体機能不全
黄体機能不全はプロゲステロン欠乏を来し、その結果反復流産の原因となり得るが、多くの場合は妊娠中のプロゲステロンの欠乏は他の原因に起因する流産の必然的、二次的結果と考えられる。不育症患者における黄体機能不全の頻度は20〜60%と報告されているが、これらは非妊娠時の話であって、すでに妊娠した患者での黄体機能を評価し得る信頼できる方法は存在しない。妊娠時の黄体は非妊娠時の黄体とは異なるので、非妊娠サイクルでの黄体機能の評価は妊娠時を反映しないといわれている。初期流産に終わった妊娠周期の着床前期の黄体ホルモン値は、妊娠成功時と比べて差が認められなかったと報告されている。また、不育症患者の非妊娠周期の高温期中間での血清プロゲステロン値を評価し、黄体機能不全のある群とない群に分けて次回妊娠の流産率を比較したところ、両群に差を認めなかったという報告もある。以上の様に黄体機能不全が流産の原因になり得るのか疑わしいにもかかわらず、ホルモン療法は広く行われている。その効果については多くの報告があるが、黄体ホルモンの補充療法については、流産の危険を減らすと言うに充分な根拠は見い出されていない。確かに、いくらかは効果がある事を示唆するデーターはあるが、証明するにはより多くの検討が必要である。
2)甲状腺機能異常
甲状腺機能異常は流産の原因としてしばしば挙げられているが、意外な事に甲状腺ホルモン値の異常が流産の原因になり得るかに関しては、その直接的な証拠は未だ無いのが現状であり、逆に最近否定的な論文が相次いで報告され注目を浴びている。しかしながら、バセドー氏病や橋本病にみられる甲状腺に対する自己抗体が反復流産の率の上昇と関係するという報告はいくつかある。その理由は不明であるが、自己免疫疾患はいくつかの自己抗体を合わせ持つ事が良くあるので、抗リン脂質抗体など他の妊娠に対して病原性のある自己抗体を介して流産が起きている可能性は否定できない。
3)高プロラクチン血症
高プロラクチン血症が反復流産の原因となり得るという説は今のところ証明されていない。多くの論文は、未治療の高プロラクチン血症の患者の流産率は高く無いと報告している。正常妊娠においてもプロラクチンレベルは妊娠初期より上昇し、非妊時の10倍に達すると報告されており、プロラクチンが直接妊娠を妨害するとは考えにくい。しかしながら、言うまでも無く高プロラクチン血症は無排卵を引き起こし、不妊症の原因となり得るので高プロラクチン血症と診断された場合は治療するべきである事は言うまでも無い。
2.不育症の分野における新しい概念
最近10年のあいだに、不育症の新しい原因や治療が見い出されてきた。多くは生殖免疫、血液凝固学の進歩によるものである。生殖免疫の領域では、Th1とTh2のバランスが崩壊する事により流産が起きるという新しく、かつ魅力的な仮説が最近注目されている。また、血液凝固の領域では、抗リン脂質抗体症候群を初めとしたthrombophiliaと不育症の関係が明らかになってきた。ここでは、それらの概念について紹介する。
1)Th1/Th2バランス
胎児は母体にとって半分は同種移植片であると考えることができるが、妊娠中は拒絶反応がおきて流産にいたらないような、なんらかの防御機構が働いていると考えられる。近年、免疫学的妊娠維持機構としてTh1/Th2バランスが注目されている。それによると、母体が胎児を異物として拒絶することなく、妊娠が維持されるのは細胞性免疫を司るCD4+ T helper (Th) 1 細胞機能が低下し、抗体産生を司るTh2細胞機能が亢進するためと考えられている。
習慣流産の免疫学的原因としては、抗リン脂質抗体など自己抗体によるものと、臓器移植の拒絶反応に準じた機序が考えられ、どちらもTh1/Th2バランスの破綻が示唆されている。すなわち、Th1/Th2バランスがTh1の方へ傾けば、母体は胎児を異物として認識し、拒絶反応がおき、流産する可能性がある。また、過剰にTh2の方へ傾くと、今度は抗体産生が盛んになり、抗リン脂質抗体などの自己抗体が産生され、流産を引き起こす可能性がある。SLEなどの自己免疫疾患が、妊娠・分娩をきっかけに発症したり増悪するのも、妊娠によりTh1/Th2バランスがTh2の方へ傾く事がきっかけとも考えらえる。
2)ナチュラルキラー(NK)細胞と不育症
この分野は最近注目され、盛んに研究されているが諸説入り乱れ、それぞれ仮説の域をでていない。実際の臨床にNK細胞に関する検査、治療を導入するのは現時点では不適切であり、現に不育症患者の間では混乱が生じている様である。
末梢血NK細胞活性は不妊症、不育症患者において高値であると報告されており、妊娠前のNK細胞活性値はその後の流産を予知すると報告されている。しかしながら、NK活性は精神的影響により変動するとも報告され、流産の結果としてストレスにより活性が上昇している可能性も否定できない。以上の様に末梢血NK細胞活性と流産との因果関係は不明であり、まして治療に関しては報告がない。
一方で、末梢血とは異なり分泌期子宮内膜や妊娠初期脱落膜にはCD56+/16-のNK細胞様のリンパ球(uNK細胞)が特徴的に増加する事が報告され、その役割についてさまざまな仮説が報告されている。最近では、uNK細胞は妊娠維持に必須であるという仮説が多くの支持を集めているが、uNK細胞が存在しないIL-2Rγ鎖KOマウスでも流産、子宮内胎児発育遅延が生じないというデータが最近報告され、注目されている。
3)thrombophiliaと不育症
血栓症の原因となり得る基礎疾患があると、pregnancy lossのリスクが高くなるというのは周知の事実である2)3)。反復妊娠初期流産患者において血液凝固系の検索を施行したところ、抗リン脂質抗体と第12因子欠乏症が2大原因として浮かび上がってきた2)7)8)。抗リン脂質抗体の多くは従来より注目されてきた抗カルジオリピン抗体やループスアンチコアグラントよりはむしろ、キニノーゲンを認識する抗フォスファチジルエタノールアミン抗体が多い4)-8)。キニノーゲンも第12因子も、カリクレイン-キニン系の蛋白であり、線溶系に重要な役割を演じている。したがって、これらに対する抗体が存在するなどして活性が低下するとカリクレイン-キニン系の破綻による線溶系低下が生じ、血栓や流産の原因と成り得る。なお、抗フォスファチジルエタノールアミン抗体は、SRLで測定可能である。
妊娠後期に子宮内胎児死亡を起こすタイプの不育症群で血液凝固系を検索すると、プロテインS欠乏、抗カルジオリピン抗体第5因子 Leiden mutationなどがrisk factorとして挙げられた3)。また、最近高ホモシステイン血症と血栓症の関係が注目されており、その原因の一つとしてmethylenetetrahydrofolate reductase(MTHFR) geneのC677T mutationが挙げられているが、このC677T mutationと上記のrisk factorの合併症例も多く、妊娠中に葉酸の必要性が増すこともあって、そのような症例では葉酸の経口摂取が勧められている3)。
3.免疫療法についての最近の考え方
胎児は母体にとって半分は同種移植片であると考えることができるが、妊娠中は拒絶反応がおきて流産にいたらないような、なんらかの防御機構が働いていると考えられる。そして、この妊娠維持機構のバランスが崩れ、流産にいたるようなタイプの不育症が存在する可能性が示唆されてきた。すなわち、Th1/Th2バランスがTh1に傾いた状態と想定される。しかしながら、胎盤という解剖学的障壁の存在や特殊な内分泌環境、サイトカインの関与など、妊娠には臓器移植とは異なるファクターも多く、臓器移植と同様にあつかうことはできない。臓器移植において、移植された臓器が拒絶されずに生着するには、白血球の血液型であるHLAの適合が重要である。同様に、妊娠維持においても夫婦間のHLAの一致、不一致が重要なのではないかという仮説が一世を風靡し、夫婦間のHLAの適合数で相性が良いとか悪いとか判定し、相性の悪い症例には夫リンパ球を用いた免疫療法が有効であるとされた。しかしながら、その後の検討により、今ではHLAの適合数と流産との相関関係は否定された。今では免疫療法は、諸検査施行しても異常の見い出されない原因不明習慣流産(2回の流産既往は適応とならない)で、抗核抗体や抗リン脂質抗体などの自己抗体を持たない症例を対象に、適応を慎重に検討したうえで施行されている。作用機序としては、Th1/Th2バランスをTh2の方へ是正すると考えられているが、否定的な論文もあり、未だ作用機序は不明である。また、副作用も報告されているので、安易に免疫療法を乱用することは慎むべきである。
おわりに
以上、不育症の最近の進歩について概説した。言うまでも無く不妊症とは全く異なる分野であり、専門的知識を要する。本稿が不育症の分野の理解に少しでもお役に立てれば幸いである。
参考文献
1)Plachot M et al. Are clinical and biological IVF parameters correlated with chromosomal disorders in early life: a multicentric study. Hum Reprod,3:627-635,1988
2)Gris JC et al. Prospective evaluation of the prevalence of haemostasis abnormalities in unexplained primary early recurrent miscarriages. Thromb Haemost, 77: 1096-103, 1997.
3)Gris JC et al. Case-control study of the frequency of thrombophilic disorders in couples with late foetal loss and no thrombotic antecedent. Thromb Haemost, 81:891-99,1999.
4) Sugi T and McIntyre JA. Autoantibodies to phosphatidylethanolamine (PE) recognize a kininogen-PE complex. Blood 86:3083-9,1995
5) Sugi T and McIntyre JA. Phosphatidylethanolamine induces specific conformational changes in the kininogens recognizable by antiphosphatidylethanolamine antibodies. Thromb Haemost 76:354-60,1996
6) Sugi T et al. Prevalence and heterogeneity of antiphosphatidylethanolamine antibodies in patients with recurrent early pregnancy losses. Fertil Steril 71: 1060-5,1999
7) Sugi T and Makino T. Plasma contact system, Kallikrein-kinin system and antiphospholipid-protein antibodies in thrombosis and pregnancy. J Reprod Immunol 47: 169-184, 2000
8) Sugi T and Makino T. Autoantibodies to contact proteins in patients with recurrent pregnancy losses. J Reprod Immunol (in press).
|
 |
2010.05.22 Saturday
 |
|
不育症における新しい概念
【参考文献】
産婦人科治療 Vol.79 No.5 (1999:11)
牧野恒久 杉 俊隆
「生殖医療の現状と展望 3.生殖のロス、習慣流産」
※文中の赤字は私が加筆した部分です。紫字は補足説明のページへのリンクが貼ってあります。ご参考までに。
--------------------------------------------------------------------------------
はじめに
不妊症の分野は近年その進歩がめざましく、体外受精などを初めとして次々と新しい治療法が開発され、10年前までは挙児をあきらめるしかなかったような夫婦でも、今では当然のように子供が授かるようになってきた。しかしながら、子宮はいまだにブラックボックスであり、着床から妊娠、分娩にいたるまでutero-placental unitで何が起きているのか、不明な点が多い。それにもかかわらず、不育症の分野もまた、最近10年で大いなる発展を遂げてきた。その内容は、生殖免疫、血液凝固学の進歩によるところが多く、高度に専門化しつつある。
本稿では、不育症について概説し、さらには最先端の知見なども併せて紹介したい。
1.不育症、習慣流産とは
不育症とは、厳密な定義をもつ医学用語ではない。強いて定義づければ、成立した妊娠を完遂できず、健康な生児に恵まれない症例を指すものといえる。一般的には習慣流産を指すことが多いが、同義ではない。習慣流産とは、3回以上流産を繰り返すことであり、時期は妊娠22週未満に限定される。しかしながら、不育症といった場合は妊娠中期以降の子宮内胎児死亡や反復流産(流産回数2回)も含まれ得る。不育症に相当する英語としては、recurrent fetal lossという表現をしばしば目にするが、fetus(胎児)という名称は妊娠10週以降に限定され、それ以前のembryo(胎芽)が含まれないので、recurrent pregnancy lossが適当であると思われる。
1回の独立した流産の頻度は統計上約15〜20%であり、決して珍しくない。その約60〜70%以上は胎児に染色体異常があると報告されている。また、受精卵の約40%に染色体異常があり、それが出生時には0.6%に減少すると報告されており、もし流産という自然淘汰が起こらなければ、出生した児の40%が染色体異常をもつことになる。したがってある意味では、流産の多くは病的ではなく、それを止めることもできないし、止める必要もないということになる。1回や2回の流産既往があっても、それがただちに病的であり、不育症であるということにはならない。ちなみに1回の独立した妊娠の流産の頻度を20%と仮定すると、反復流産率は0.2×0.2=0.04で4%、3回流産率は0.04×0.2=0.08で0.8%となる。したがって、反復流産の場合は病的原因のもたず、不育症とはいえない場合も多いが、3回以上自然流産を繰り返した習慣流産の場合は自然淘汰という考えでは確率的に説明できず、不育症の原因を検索することになる。
2.不育症の検査、原因、治療
不育症の原因は多岐にわたっており、系統だてて諸検査を施行し、総合的に判断して方針を決定する必要がある。表1は不育症一般検査を示したものである。これらの諸検査を施行した結果、表2のような結果が得られている。もちろん、これらは不育症一般検査の異常とその頻度を示したものであり、習慣流産の原因とその頻度という訳ではない。数年前の不育症の原因頻度としては、われわれの印象では、内分泌異常が約10%、子宮内腔異常が約15%、染色体異常が約10%、自己抗体が約20%、原因不明が約45%である。しかしながら、最近10年のこの分野の進歩により、原因不明の頻度は約45%から20%ぐらいにまで減少した印象がある。
不育症の治療について、まず最初に、すでに治療方針がある程度確立している古典的なものについて概説する。
表1 不育症一般検査
1.問診、基礎体温
2.感染症検査
クラミジアDNA、子宮頸部・膣内培養
血算、血沈、CRP
3.内分泌検査
下垂体機能(プロラクチン)
黄体機能(黄体ホルモン、子宮内膜組織検査)
甲状腺機能(freeT3、freeT4、TSH)
糖尿病検査(空腹時血糖)
4.子宮形態異常
子宮卵管造影、子宮鏡、超音波検査
5.夫婦染色体検査
6.免疫学的検査
抗核抗体、抗DNA抗体、RF
抗リン脂質抗体、Lupus Anticoagulant
不規則抗体検査
7.血液凝固系検査
血小板凝集能、aPTT、TAT
protharombin F1+2、第12因子
表2 習慣流産の検査異常とその頻度(%)
子宮内腔異常
弓状子宮 11.9
双角または中隔子宮 5.2
Asherman症候群 1.4
単角子宮 0.5
重複子宮 0.3
子宮筋腫 1.1
免疫学的異常
抗リン脂質抗体 12.1
aPTT延長 7.5
抗核抗体 22.0
リウマチ因子 4.2
染色体異常
妻 5.8
夫 3.9
感染症
クラミジア抗原 0.8
内分泌異常
高プロラクチン血症 15.1
甲状腺機能低下症 4.1
甲状腺機能亢進症 1.2
糖尿病 0.2
2−1.感染
血液検査で炎症の兆候がないかを検索するとともに、クラミジア頸管炎および子宮頸部・膣内培養(目標菌:B群溶連菌)を施行する。クラミジア抗体検査は過去の感染でも陽性にでるなど、治療の適応、効果判定に関しては問題がある。妊娠への直接的関係を調べるためには子宮頸部から直接検体を採取する方が望ましい。陽性にでれば、起因菌に対応す抗生剤で治療する。ただし、B群溶連菌やクラミジアなどの個々の病原菌が直接流産の原因になり得るかに関しては、証明されていない。
2−2.甲状腺機能異常
甲状腺機能異常の患に初期流産が多いことは以前より知られていたが、われわれの統計では習慣流産患者の約5%に機能異常が認められる。甲状腺機能低下症は二次的に高プロラクチン血症を引き起こすため、高プロラクチン血症を介した機序も考えられる。治療としては、機能亢進症に対してはmercazoleやpropylthiouracil、機能低下症に対してはtyradin Sなどである。propylthiouracilとtyradin Sには胎盤通過性はない。melcozoleに関しては、胎盤通過性はあるものの、最近の報告ではヒトでの催奇形性に関しては有意な差はないといわれている。
2−3.高プロラクチン血症
習慣流産患者の約15%に認められる。潜在性高プロラクチン血症も考慮して、疑わしい時はTRH testも考慮する。THR testでは、負荷後15分でプロラクチン値70ng/ml以上を陽性とする。甲状腺機能と関連が強いので妊娠中も含めて両者を見ながら治療することが望ましい。下垂体腺種が存在する場合は脳外科に依頼する。治療としてはパーロデルやテルロンの投与を行う。下垂体腺種がある場合、手術前にパーロデルを投与すると手術がやりにくくなるので、脳外科と相談して手術の適応を検討したうえで投与を決定する。また、当然向精神薬などの副作用による薬剤性高プロラクチン血症は否定しておく。
2−4.黄体機能不全
高温期の中間でプロゲステロン値が10ng/ml未満なら治療の対象となる。黄体ホルモン経口または経膣投与やhCG筋注にて補充する。ただし、黄体機能不全が真に流産を惹き起こすかに関しては、否定的な報告もある。
2−5.糖尿病
空腹時血糖値が高い場合は75gGTT(ぶどう糖負荷検査)を行う。妊娠初期にコントロールできていないと胎児奇形を引き起こす可能性があるので、コントロールがついてから妊娠を許可する。実際の習慣流産患者での糖尿病の頻度は低い。
2−6.子宮形態異常
子宮卵管造影にて子宮奇形、子宮筋腫、Asherman症候群などの有無を見る。子宮内腔の形態が重要なので、バルーン法でなく、嘴管を用いて造影することが望ましい。異常と思われる陰影が得られた時は、必要に応じて子宮鏡検査を施行する。また中隔子宮を双角子宮の識別は子宮内腔の検査では困難なので、超音波断層法、MRIや腹腔鏡にて子宮の外形を観察し、診断する。個々の形態異常の程度にもよるが、一般的に中隔子宮の流産率が最も高く、単角、双角、重複、弓状子宮等がそれに続く。子宮奇形の治療としては子宮形成術が適応となり、Strassmann, Jones&Jones, Tompkinsなどの開腹手術やResectoscopeを用いた経膣手術(TCR;trans cervial resection)が行われる。TCRは中隔子宮場合に有用であるが、子宮穿孔の危険があり、腹腔鏡での監視が必要で熟練を要するため、実施できる施設は限られるという欠点がある。
2−7.染色体異常
女性側の染色体異常における理論的流産率はロバートソン転座で4/6(67%)、相互転座で2/4(50%)である。モザイクはその比率によって流産率は異なる。いうまでもなく治療は不可能であるので、理論的流産率などに基づいたカウンセリングを行う。
3.不育症分野における新しい概念
最近10年のあいだに、不育症の新しい原因や治療が見出されてきた。多くは生殖免疫、血液凝固学の進歩によるものである。生殖免疫の領域ではTh1とTh2のバランスが崩壊することにより流産が起きるという新しく、かつ魅力的な仮説が最近注目されている。また、血液凝固の領域では、抗リン脂質抗体症候群を初めとしたthrombophilia(血栓形成傾向)と不育症との関係が明らかになってきた。ここでは、それらの概念について紹介する。
3−1.Th1/Th2バランス
胎児は母体にとって半分は同種移殖片であると考えることができるが、妊娠中は拒絶反応が起きて流産に至らないような、何らかの防御機構が働いていると考えられる。近年、免疫学的妊娠維持機構としてTh1/Th2バランスが注目されている。それによると、母体が胎児を異物として拒絶することなく、妊娠が維持されるのは細胞性免疫を司るCD4+T helper(Th)1細胞が低下し、抗体産生を司るTh2細胞機能が亢進するためと考えられている。
習慣流産の免疫学的原因としては、抗リン脂質抗体など自己抗体によるものと、臓器移植の拒絶反応に準じた機序が考えられ、どちらもTh1/Th2 バランスの破綻が示唆されている。すなわち、Th1/Th2バランスがTh1の方へ傾けば、母体は胎児を異物として認識し、拒絶反応が起き、流産する可能性がある。また、過剰にTh2の方へ傾くと、今度は抗体産生が盛んになり、抗リン脂質抗体などの自己抗体が産生され、流産を引き起こす可能性がある。SLEなどの自己免疫疾患が、妊娠分娩をきっかけに発症したり増悪するのも、妊娠によりTh1/Th2 バランスがTh2の方へ傾くことがきっかけとも考えらえる。(Th1/Th2に関しては未だ研究段階にあり、東海大の不育外来においても、一般検査項目には含まれていないとのこと。)
3−2.thrombophlia
血栓症の原因となり得る基礎疾患があると、 pregnancy loss のリスクが高くなるというのは周知の事実である。反復妊娠初期流産患者において血液凝固系の検索を施行したところ、抗リン脂質抗体と第12因子欠乏症が2大原因として浮かび上がってきた。 抗リン脂質抗体の多くは従来より注目されてきた抗カルジオリピン抗体やループスアンチコアグラントよりはむしろ,キニノ一ゲンを認識する抗フォスファチジルエタノ−ルァミン抗体が多い。キニノーゲンも第12因子も、カリクレイン−キニン系の蛋白であり、線溶系に重要な役割を演じている。したがって、これらに対する抗体が存在するなどして活性が低下するとカリクレイン一キニン系の破綻による線溶系低下が生じ、血栓や流産の原因と成り得る。なお、抗フォスファチジルエタノ−ルァミン抗体は、SRLで測定可能である。
妊娠後期に子宮内胎児死亡を起こすタイブの不育症群で血液凝固系を検索すると、プロテインS欠乏、抗カルジオリピン抗体、第5因子Leiden mutationなどが risk factorとして挙げられた。また、最近高ホモシステイン血症と血栓症の関係が注目されており、その原因の一つとして methylenetetrahydrofolate reductase(MTHFR)geneの C677T mutation(ホモシステイン代謝に関与する酵素の677番目の遺伝子の突然変異)が挙げられているが、このC677T mutationと上記のrisk factorの合併症例も多く、妊娠中に葉酸の必要性が増すこともあって、そのような症例では葉酸の経口摂取が勧められている。
4.不育症の分野における最近のトピックス
4−1.免疫療法
胎児は母体にとって半分は同種移植片であると考えることができるが、妊娠中は拒絶反応が起きて流産に至らないような、何らかの防御機構が働いていると考えられる。そして、この妊娠維持機構のバランスが崩れ、流産に至るようなタイプの 不育症が存在する可能性が示唆されてきた。すなわち、Th1/Th2バランスがTh1に傾いた状態と想定される。しかしながら、胎盤という解剖学的障壁の存在や 特殊な内分泌環境、サイトカインの関与など、妊娠には臓器移植とは異なるファクタ一も多く、臓器移植と同様に扱うことはできない。 臓器移植において、移植された臓器が拒絶されずに生着するには、白血球の血液型であるHLAの適合が重要である。同様に、妊娠維持においても夫婦間のHLAの一致、不一致が重要なのではないかという仮説が一世を風靡し、夫婦間のHLAの適合数で相性が良いとか悪いとか判定し、相性の悪い症例には夫リンパ球を用いた免疫療法が有効であるとされた。しかしながら、その後の検討により、今ではHLAの適合数と流産との相関関係は否定された。今では免疫療法は、諸検査施行しても異常の見い出されない原因不明習慣流産 (2回の流産既往は適応とならない)で、抗核抗体や抗リン脂質抗体などの自己抗体を持たない症例を対象に、適応を慎重に検討したうえで施行されている。作用機序としては、Th1/Th2バランスをTh2の方へ是正すると考えられている。副作用も報告されているので、安易に免疫療法を乱用することは慎むべきである。
4−2.抗リン脂質抗体
抗リン脂質抗体とは,リン脂質に対する自己抗体であり、具体的には電気的陰性のリン脂質(カルジオリピン、フォスファチジルセリン、フォスファチジルグリセロール、フォスファチジルイノシトール、フォスファチジン酸など)や,電気的中性のリン脂質(フォスファチジルエタノ−ルアミン、フォスファチジルコリン)に対する抗体であると考えられていた。
抗リン脂質抗体と一言でいっても、その実体は実に複雑であり、それが抗リン脂質抗体の理解を困難にしている。抗リン脂質抗体という名前がまず誤解を生む源であり、従来は名前どおりリン脂質を認識する抗体であると思われてきたが、最近、その多くは、実はリン脂質そのものを認識する抗体ではなく、リン脂質に結合する血漿蛋白に対する抗体であるということが分かってきた。最初に発見された抗原は、β2-glycoproteinI(β2GPI) であり、次いで、プロトロンビンが報告された。これらは、カルジオリピンやフォスファチジルセリンなど、電気的陰性のリン脂質に対する抗体の対応抗原である。その後われわれは、中性のリン脂質であるフォスファチジルェタノ−ルアミンに対する抗体も同様にリン脂質結合蛋白を認識することを発見し、それがキニノ−ゲンであることを同定した。 このように、抗リン脂質抗体といっても実はまったく異なる抗体の総称であり、共通点はリン脂質に結合する蛋白を認識するということだけである。したがって、それぞれの病原性およびその機序は異なると考えられる。
近年、抗リン脂質抗体と反復流産、反復血栓症、血小板減少症との関係は広く知られており、抗リン脂質抗体症候群と称され、注目を浴びている。抗リン脂質抗体症候群は、関連する全身疾患をもたないprimary抗リン脂質抗体症候群と、SLEやその他の膠原病を伴うsecondary抗リン脂質抗体症候群に分けられる。妊娠に関しては、中期以降の子宮内胎児死亡がもっとも抗リン脂質抗体に特徴的である。胎盤の血栓が原因といわれているが、因果関係はいまだ不明である。また、妊娠初期の反復流産も抗リン脂質抗体と関係している。
治療としては,低用量ァスピリン療法やへパリン療法が広く行われている。また、症例によってはプレドニゾロンが投与されることもある。詳しくは他稿を参照されたい。
抗リン脂質抗体症候群は最近非常に注目されている分野であり、次々と新しい抗体が発見され、治療法も確立されつつある。検査法の確立により、今まで原因不明とされていた不育症の多くが治療可能になることが期待される。
おわりに
以上概説したように、不育症の分野は多分に内科的であり、緻密な診断、治療が不可欠である。最近では原因不明不育症の頻度も著明に減少し、 多くの患者が無事赤ちゃんを抱いて退院していくようになった。しかしながら、現代の核家族化による情報不足もあり、一度や二度の流産で深刻な精神的打撃を受け、孤立している夫婦も多い。流産や不育症についての情報を一層社会に広めるとともに、不育症の専門外来では飛躍的な進歩により、多くの不育症の患者が治療可能であるという事実に患者も産婦人科医も理解を深めたい。
|
 |
2010.05.22 Saturday
 |
|
妊娠維持と自己抗体
【参考文献】
MBL 自己免疫レポート No.29 Aug.2002より
妊娠維持と自己抗体
東海大学医学部母子生育学系産婦人科学部門
杉 俊隆、牧野恒久 注)青字は私smileが加筆した部分です。
--------------------------------------------------------------------------------
1. 習慣流産、不育症における免疫・血液凝固学の位置付け
以前よりSLEをはじめとする自己免疫疾患の患者にpregnancy lossが多いことが知られ、母体の免疫能の異常が妊娠維持に障害を起こす可能性が指摘されてきた。最近になって、それが抗リン脂質抗体という自己抗体によって惹き起こされるという説が注目されるようになり、抗リン脂質抗体と関連する不育症、血栓症をまとめて抗リン脂質抗体症候群と称し、広く認知されるようになった(表1)。不育症とならんで血栓症がその症候群の診断基準案1)に列挙されたということは、不育症の病因として免疫だけではなく、免疫・血液凝固学的機序が存在する可能性が示唆されたことになる。また一方で、以前より血栓傾向のある患者に胎盤血栓によると思われるpregnancy lossが多いことも指摘されており、近年、血栓性素因(thrombophilia)と不育症の関係も解明されつつある。thrombophiliaには先天的血栓傾向を示す疾患と、後天的な疾患がある。後天的thrombophiliaの代表的なものは抗リン脂質抗体症候群であり、先天的thrombophiliaの中には、アンチトロンビン、プロテインC、プロテインSなどの抗凝固因子の先天性欠乏症や、活性化プロテインCに対して抵抗性を示す第5因子Leiden mutationなどがある。
近年、フランスのグループ(NOHA; The Nimes Obstetricians and Haematologists)が不育症と血液凝固の関連について大規模な調査を行い、興味深い結果を発表している(NOHA study)2,3)。これによると、妊娠初期流産を繰り返しているタイプの不育症と、妊娠後期のfetal lossを起こすタイプの不育症では、その血液凝固異常の傾向が異なる。
妊娠初期流産を繰り返すタイプの不育症では線溶系の低下が多く見られ(約40%)、その内容は主にplasminogen activator inhibitor 1 (PAI)活性亢進であった。具体的には、第12因子欠乏症(9.4%)と抗リン脂質抗体(7.4%)が流産の2大risk factorとして報告されており、我々の不育症外来でも同様の結果が得られている。第12因子はカリクレイン-キニン系の一員であり(図1)、線溶系に重要な役割を果たしている。したがって、第12因子の欠乏は線溶系の低下を惹き起こし、血栓症、流産の原因となり得る4)。また、抗リン脂質抗体に関する最近のデータによると、妊娠初期流産を繰り返すタイプの不育症群では抗フォスファチジルエタノールアミン抗体(抗PE抗体)が多く見い出され、その多くはキニノーゲンを認識するタイプの抗PE抗体であった5-7)。キニノーゲンもまた第12因子と同様カリクレイン-キニン系の蛋白であり、それに対する自己抗体が存在すると線溶系を低下させる可能性がある。以上をまとめると、妊娠初期流産を繰り返すタイプの不育症の血液凝固学的特徴は線溶系の低下とまとめる事ができる。
これに対して妊娠後期のfetal lossを起こすタイプの不育症では、抗リン脂質抗体、プロテインS欠乏症、第5因子Leiden mutationがリスクファクターとして挙げられた3)。抗リン脂質抗体の病原性は今だ不明の点が多いが、抗カルジオリピン抗体はプロテインS、プロテインC経路を阻害するという説もあり、妊娠後期のfetal lossを起こすタイプの不育症の血液凝固学的特徴は、トロンボモジュリン/プロテインC/プロテインS/第5因子系の破綻とまとめることが出来るかもしれない。ただし、日本では今のところ第5因子Leiden mutationの報告は無い。
表1 抗リン脂質抗体症候群診断基準案(1998;札幌Criteria)
臨床所見:
血栓症: 1回またはそれ以上の
・動脈血栓
・静脈血栓
・小血管の血栓症(組織、臓器を問わない)
妊娠の異常:
・3回以上の連続した原因不明の10週未満の流産(解剖学的、遺伝的、内分泌学的原因を除く)
・1回以上の胎児形態異常のない10週以上の原因不明子宮内胎児死亡
・1回以上の新生児形態異常のない34週以下の重症妊娠中毒症または重症胎盤機能不全に関連した早産
検査所見:
抗カルジオリピン抗体
・IgGまたはIgM
・中、高抗体価
・6週間以上の間隔をあけて、2回以上陽性
・β2-glycoprotein I 依存性抗カルジオリピン抗体を検出し得る標準化されたELISAで測定
ループスアンチコアグラント
・6週間以上の間隔をあけて、2回以上陽性
・International Society on Thrombosis and Hemostasisのガイドラインに従って検出
臨床所見が1つ以上、検査所見が1つ以上存在した場合、抗リン脂質抗体症候群と診断する
2. 抗リン脂質抗体の多様性
近年、抗リン脂質抗体と不育症との関係が注目を浴びている。抗リン脂質抗体とはリン脂質に対する自己抗体であり、具体的には電気的陰性のリン脂質(カルジオリピン、フォスファチジルセリン、フォスファチジルグリセロール、フォスファチジルイノシトール、フォスファチジン酸)や、電気的中性のリン脂質(フォスファチジルエタノールアミン、フォスファチジルコリン)に対する抗体である。
歴史的には、抗リン脂質抗体は梅毒血清反応陽性として検出されてきた。梅毒血清反応では、抗原としてカルジオリピンが使用されており、したがって陽性とはカルジオリピンに対する抗体の存在を示している。梅毒ではないのに抗カルジオリピン抗体をもつ患者の場合、梅毒血清反応の生物学的偽陽性として抗リン脂質抗体が検出された訳である。抗リン脂質抗体は歴史的に梅毒反応偽陽性として発見されたため、抗カルジオリピン抗体が最も有名である。しかし、実際には細胞膜リン脂質の構成成分にカルジオリピンは存在しない(図2省略)。cardio(心臓の)-lipin(脂質)という名前の通りカルジオリピンは心臓に豊富に存在し、有核細胞ではミトコンドリアの内側にのみ存在する。細胞膜の構成成分としての陰性荷電リン脂質は、フォスファチジルセリン(PS)とファオスファチジルイノシトールであるが、比較的少ない。むしろ中性荷電リン脂質が主要な細胞膜の構成成分であり、フォスファチジルエタノールアミン(PE)やフォスファチジルコリン(PC)、スフィンゴミエリン(SM)がある(図2)。細胞は活性化されるとその細胞膜リン脂質の構成を変化させる8)。すなわち静止期では中性荷電が主に細胞膜外側に存在するが、活性化すると陰性荷電が細胞膜外側に移動する(図2)。したがって、陰性荷電リン脂質に対する抗体が静止期の血小板や血管内皮細胞を認識し、活性化させるということは考え難い。
抗リン脂質抗体と一言で言っても、その実体は単純ではない。従来は名前どおりリン脂質を認識する抗体であると思われてきたが、最近、病原性のある抗体の多くは、実はリン脂質そのものを認識する抗体ではなく、リン脂質に結合する血漿蛋白に対する抗体であるということが分かってきた。一番最初に発見された抗原は、β2-glycoprotein I(β2GPI)であり、当初はコファクターと称されたが、その後は事実上の抗カルジオリピン抗体の目標抗原ということでコンセンサスが得られている。次いで、プロトロンビンが報告された。これらは、カルジオリピンやフォスファチジルセリンなど、電気的陰性のリン脂質に対する抗体の対応抗原である9-12)。その後我々は、中性のリン脂質であるフォスファチジルエタノールアミンに対する抗体も同様にリン脂質結合蛋白を認識することを発見し、それがキニノーゲンであることを同定した7)。したがって、厳密にいえばこれらの抗体を抗リン脂質抗体と呼ぶのは誤りであり、それぞれ抗β2GPI抗体、抗プロトロンビン抗体、抗キニノーゲン抗体などと呼ぶべきである。しかしながら、歴史的に抗リン脂質抗体と呼ばれていたために、現在もそのままになっている。
抗カルジオリピン抗体をELISA法で検出する際に、免疫グロブリンの非特異的結合を抑制するためにウシ血清を加えるのが一般的であるが、このウシ血清中にβ2GPIを始めとしたリン脂質結合蛋白が含まれており、抗カルジオリピン抗体を検出したつもりでも、実際はカルジオリピンに結合したβ2GPIを認識する抗体を検出していたわけである。しかしながら、多くの所謂“抗カルジオリピン抗体”はβ2GPIが単独で存在した場合は認識せず、カルジオリピンに結合して立体構造の変化をおこして抗原性の変化したβ2GPIしか認識しないことから、“抗カルジオリピン抗体”の検出には依然としてカルジオリピンの存在が必須であるために、抗β2GPI抗体とは改名されずに今日に至っているわけである。ちなみに、梅毒患者のもつ抗カルジオリピン抗体はカルジオリピンそのものを認識する抗体であり、血栓症などの病原性は報告されていない。この様な、本当の抗カルジオリピン抗体はβ2GPI非依存性抗カルジオリピン抗体と呼ばれ、β2GPIを認識する抗カルジオリピン抗体(β2GPI依存性抗カルジオリピン抗体)と区別しているのが現状である。
我々が報告した、キニノーゲンを認識する抗フォスファチジルエタノールアミン抗体(抗PE抗体)の場合も同様であり、抗PE抗体はカルジオリピン(CL)、フォスファチジルセリン(PS)、フォスファチジルコリン(PC)など、他のリン脂質と結合したキニノーゲンや、フリーのキニノーゲンを認識しないが、PEに結合したキニノーゲンだけを認識する(図3省略)13)。これは、キニノーゲンがPEと結合すると、特異的な立体構造の変化が生じ、新しいエピトープがキニノーゲン上に出現し、それを抗PE抗体が認識するという事を意味する。したがって、単純に抗キニノーゲン抗体と呼べず、キニノーゲン依存性抗PE抗体と呼んでいるのが現状である。
このように、抗リン脂質抗体といっても実は全く異なる血漿蛋白を認識する抗体の総称であり、共通点はリン脂質に結合する蛋白を認識するということだけである。したがって、それぞれの病原性は認識するリン脂質結合蛋白によって異なると考えられる。
3. キニノーゲンを認識する抗リン脂質抗体
抗カルジオリピン抗体やループスアンチコアグラントに特徴的なのは、妊娠中期以降の子宮内胎児死亡である。しかしながら、臨床で一番多く見られるのは妊娠初期流産を繰り返す不育症であり、そのような患者に対して抗カルジオリピン抗体やループスアンチコアグラントを検査しても陽性にでることは期待するほどは多くない。我々は、妊娠10週未満の流産を繰り返す反復初期流産患者139人に対して、抗リン脂質抗体のスクリーニングを施行したところ、陰性荷電リン脂質を認識する抗カルジオリピン抗体、抗フォスファチジルセリン抗体、ループスアンチコアグラントに関しては、患者群と正常対照群で陽性率に差を認めなかったが、抗PE抗体はIgGが20.1%、IgMが12.2%、IgAが1.4%の陽性率であり、正常対照群と比較して統計学的に有意(p=0.0002)であった5)。したがって、反復初期流産患者にもっとも多く見られる抗リン脂質抗体は抗PE抗体であるという結論に達した。この事は我々が1999年に発表し、2000年になってフランスのGrisらによって同様の結果が報告された6)。さらに、不育症患者の持つPE結合蛋白依存性抗PE抗体の90.5%はキニノーゲンを認識する事が明らかになった5)。また、抗PE抗体と流産だけでなく、抗PE抗体と血栓症との関係も報告されている14-18)。
さらに抗PE抗体がキニノーゲンのどの部位を認識しているのか、合成ペプチドを用いてepitope mappingを行ったところ、約70%の抗PE抗体は、キニノーゲン、ドメイン3のLeu331-Met357 (LDC 27)を認識する事が明らかになった19)。さらに、LDC27を2つに分け、Cys333-Lys345 (CNA13)とIle346-Met357 (IYP12)を用いて検討したところ、Cys333-Lys345 (CNA13)のみを認識した。
LDC27 LDCNAEVYVVPWEKKIYPTVNCQPLGM
CNA13 CNAEVYVVPWEKK
IYP12 IYPTVNCQPLGM
この部位は、cystein proteinase inhibitorであるキニノーゲンが血小板上のcystein proteinaseであるcalpainに結合し、血小板活性化を抑制している部位と一致する(図4)20)。従って、抗PE抗体が結合することによりcalpainに結合できなくなり、キニノーゲンのcystein proteinase inhibitor活性が阻害されると考えられ、抗PE抗体のカリクレイン-キニン系を介した病原性を強く示唆している。
さらに我々は、抗PE抗体がキニノーゲンを認識する事により、その血小板活性化を抑制する作用を阻害し、血栓の原因となり得るかに関して、in vitroの検討を行った。キニノーゲンを認識する抗PE抗体IgGと、対照としてキニノーゲンを認識しない抗PE抗体IgGをresting 血小板に加え、トロンビンで刺激したところ、キニノーゲンを認識する抗PE抗体IgGを加えた血小板に著明な血小板凝集能の亢進が観察された(図5省略)21,22)。
4. 第12因子に対する自己抗体
近年、フランスのグループ(NOHA; The Nimes Obstetricians and Haematologists)が500人の原因不明妊娠初期反復流産患者に対して血液凝固異常の有無について大規模な調査を行い、興味深い結果を発表している(NOHA study)2)。これによると、妊娠初期流産を繰り返すタイプの不育症では線溶系の低下が多く見られ(約40%)、その内容は主にplasminogen activator inhibitor 1 (PAI)活性亢進であった。具体的には、第12因子欠乏症(9.4%)と抗リン脂質抗体(7.4%)が2大危険因子として報告されており、我々の不育症外来でも同様の結果が得られている。さらに、その後抗リン脂質抗体の内訳に関する検討が同じグループにより行われ、我 Xの不育症外来と同様、抗PE抗体が最も高頻度に見られたと報告されている。
さて、抗PE抗体、すなわちキニノーゲンを認識する抗体とならんで、第12因子欠乏症が高頻度に見られた事は非常に興味深い。なぜならば、キニノーゲンも第12因子も同じカリクレイン-キニン系、またはplasma contact systemの蛋白であるからである。
第12因子欠乏症が反復血栓症の患者に多いということは以前より知られていた。反復動脈血栓または心筋梗塞患者の20%、反復静脈血栓症患者の8%に第12因子欠乏症が存在すると報告されている23)。第12因子欠乏症における血栓形成の原因として、ブラジキニン産生が減少することにより血管内皮細胞からのtissue plasminogen activator (tPA)の分泌が減少するためではないかと推測されている24)。そして、10年程前より第12因子欠乏症と反復流産との関係が報告されるようになった25)。
我々の不育症外来においては、191人の不育症患者をスクリーニングしたところ、34人(17.8%)が第12因子活性60%未満であった。一方、正常対照群60人中第12因子活性60%未満であったのは1人であった。非常に興味深い事に、第12因子欠乏症患者34人中18人(52.9%)が何らかの自己抗体陽性(主に抗リン脂質抗体と抗核抗体)であり、13人(38.2%)は抗リン脂質抗体陽性であった。このことより、第12因子欠乏には自己抗体が関与している事が強く示唆された。
最近になって、抗リン脂質抗体陽性患者に第12因子欠乏症が高頻度に存在すると言う報告がされた26)。また、第12因子に対する自己抗体が存在する事により、免疫複合体が形成され、第12因子欠乏症が起こるのではないかという仮説が提唱された。その後、抗リン脂質抗体陽性患者において、第12因子に対する自己抗体の存在が報告された27)。次いで我々も、第12因子欠乏不育症患者において第12因子に対する自己抗体の存在を報告した28,29)。第12因子は抗リン脂質抗体陽性患者の持つ自己抗体の認識する抗原のリストに加えるべきかもしれない。
5. 内因性凝固系は生体内には存在しない
カリクレイン-キニン系は、第12因子、プレカリクレイン、キニノーゲンの3つの血漿蛋白より成り立っている(図1)。これらの蛋白はまた、plasma contact systemを構成する蛋白でもある(図6)。すなわち、これらの蛋白が陰性荷電の表面に集合することにより、内因系血液凝固カスケードが開始される訳である。これらの蛋白が欠損すると、試験管内では血液は凝固せず、aPTTは延長する。しかしながら、生体内では出血傾向は見られず、逆に血栓症の危険因子となることが知られている。つまり、内因系血液凝固カスケード(contact factor pathway)は試験管の中では存在しても、生体内ではごく一部の例外を除いて存在しないということが最近になって分かってきたのである30)。
そもそも内因系の血液凝固というのは、血液がガラス表面に接触することにより発見され、1958年にMargolisらによって報告された31)。その後、kaolin、ellagic acid、dextran sulfateなどもcontact activationを引き起こすことが報告された32)。しかしながら、これらの物質は生体内には存在しないわけで、生体内でcontact activationを引き起こしている陰性荷電の表面というのは何であるか不明であった。コラーゲンが引き起こしていると長い間考えられてきたが、最近になって否定された32)。また、破綻した血管内皮細胞の表面に露出した基底膜がそうであろうと言う説もあるが、未だ証明されていない。唯一生体内で内因系血液凝固を引き起こす事が証明されているものはエンドトキシンである33-35)。しかしながら、これはseptic shockにおける内因系血液凝固しか説明できない。結局、結論として生体内にはcontact activationを引き起こすような生理的陰性荷電の表面は存在せず、実際はcontact proteinは陰性荷電の表面ではなく血管内皮細胞上に集合しており、必ずしも生体内ではcontact activationを引き起こすために陰性荷電の表面は必要ないということが明らかになってきた4)。
従って、リン脂質という陰性荷電の物質を加える事により試験管内で内因系血液凝固を引き起こして凝固時間を測定する検査であるaPTTと、生体内で起きている反応は異なる訳である。例えば、第・因子(Hageman factor)の先天性欠損症患者であるJohn Hagemanや、キニノーゲンの先天性欠損症患者であるMayme Williams (Williams trait)は両者とも出血傾向ではなく、反対の肺塞栓症で死亡したのは有名な話である。また、ループスアンチコアグラントは試験管内ではaPTTを延長させるが、生体内では血栓症を引き起こすという事も、内因系血液凝固系が生体内ではそのまま通用しない事を証明している。
6. カリクレイン-キニン系と妊娠
女性の生殖系は、体内で2番目にキニノーゲンおよびその代謝産物の豊富な部位である。ラットでは、各臓器のキニノーゲンの濃度は、血漿12.2μg/ml、子宮10.9μg/ml、肝臓0.4μg/ml、腎臓1.2μg/mlと報告されている36)。また、生殖器の組織および血漿中のキニノーゲンの濃度は、排卵、妊娠、出産で変動すると報告されている36,37)。
カリクレイン-キニン系は胎児、胎盤の血管に存在していることが最近明らかになってきている38,39)。胎盤の大きな血管や臍帯ではなく、絨毛の毛細血管内皮細胞にキニノーゲンやプレカリクレイン、カリクレインが存在する事が報告されており40)、キニンが胎盤の毛細血管に限局して産生されていることが示唆されている41)。キニンは抗凝固、線溶促進作用だけでなく、血流を増加させるなどの生物学的活性をもったペプチドであり、胎盤内で放出され、胎盤の血流や代謝産物の経胎盤輸送などを調節する重要な役割を担っている可能性が指摘されている。カリクレイン-キニン系は、全身の血液凝固、線溶系のみならず、特に生殖に非常に重要な位置を占めていると考えられる。
最近、カリクレイン-キニン系の蛋白の欠乏と反復流産との関係が報告されている。また、カリクレイン-キニン系蛋白に対する自己抗体と反復流産との関係も報告されている42,43)。カリクレイン-キニン系は、妊娠維持に重要な役割を果たしているので、その破綻は流産に直結するのかもしれない。
7. おわりに
Utero-placental unitにおいて、免疫と血液凝固系は妊娠維持機構の中で非常に重要な位置を占めている。SLEなどの基礎疾患を伴わない原発性抗リン脂質抗体症候群における不育症の治療としては、従来のステロイドを用いた免疫抑制療法は副作用が多くて次第に行われなくなり、それに代わって抗血小板療法である低用量アスピリン療法や、抗凝固療法であるヘパリン療法がfirst choiceとして取り入れられ、非常に効果を挙げている。しかしながら、このような凝固系に対する治療が広く行われるようになったにも関わらず、生殖医学における血液凝固的アプローチは今まであまりされていなかった。本稿では免疫学のみならず、血液凝固系およびカリクレイン-キニン系と免疫の関わりという新しい角度から生殖における最近の新しい知見について解説した。
参考文献
1) Wilson WA, Gharavi AE, Koike T, et al: International consensus statement on preliminary classification criteria for definite antiphospholipid syndrome. Arthritis Rheum 42:1309-11, 1999.
2) Gris JC, Neveu SR, Maugard C et al: Prospective evaluation of the prevalence of haemostasis abnormalities in unexplained primary early recurrent miscarriages. Thromb Haemost 77: 1096-1103, 1997.
3) Gris JC, Quere I, Monpeyroux F et al: Case-control study of the frequency of thrombophilic disorders in couples with late foetal loss and non-thrombotic antecedent. Thromb Haemots 81: 891-99, 1999.
4) Colman RW, Schmaier AH: Contact system: A vascular biology modulator with anticoagulant, profibrinolytic, antiadhesive, and proinflammatory attributes. Blood 90: 3819-3843, 1997.
5) Sugi T, Katsunuma J, Izumi S, et al: Prevalence and heterogeneity of antiphosphatidylethanolamine antibodies in patients with recurrent early pregnancy losses. Fertil Steril 71: 1060-65, 1999.
6) Gris JC, Quere I, Sanmarco M, et al: Antiphospholipid and antiprotein syndromes in non-thrombotic, non-autoimmune women with unexplained recurrent prmary early foetal loss. Thromb Haemost 84: 228-236, 2000.
7) Sugi T & McIntyre JA: Autoantibodies to phosphatidylethanolamine (PE) recognize a kininogen-PE complex. Blood 86: 3083-3089, 1995.
8) Bevers EM, Comfurius P, Zwaal RFA: Changes in membrane phospholipid distribution during platelet activation. Bioch Biophy Acta 736:57-66, 1983.
9) McIntyre JA, Wagenknecht DR, Sugi T. Phospholipid binding plasma proteins required for antiphospholipid antibody detection - an overview. Am J Reprod Immunol 37: 101-110, 1997.
10) Wagenknecht DR, Sugi T, McIntyre JA. The evolution, evaluation and interpretation of antiphospholipid antibody assays. Clin Immunol Newsletter, 15: 28-38, 1995.
11) Sugi T, McIntyre JA. Plasma proteins required for antiphospholipid antibody detection. Neuv Rev Fr Hematol, 37 (Suppl II): S49-52, 1995.
12) Roubey RAS. Autoantibodies to phospholipid-binding plasma proteins: A new view of lupus anticoagulant and other "antiphospholipid" autoantibodies. Blood 1994; 84: 2854-67.
13) Sugi T & McIntyre JA: Phosphatidylethanolamine induces specific conformational changes in the kininogens recognizable by antiphosphatidylethanolamine antibodies. Thromb Haemost 76: 354-360, 1996.
14) Sanmarco M, Alessi MC, Harle JR, Sapin C, Aillaud MF, Gentile S, Juhan-Vague I, Weiller PJ. Antibodies to phosphatidylethanolamine as the only antiphospholipid antibodies found in patients with unexplained thromboses. Thromb Haemost 85: 800-805, 2001.
15) Balada E, Ordi-Ros J, Paredes F, Villarreal J, Mauri M, Vilardell-Tarres M. Antiphosphatidylethanolamine antibodies contribute to the diagnosis of antiphospholipid syndrome in patients with systemic lupus erythematosus. Scand J Rheumatol 30: 235-41, 2001.
16) McIntyre JA & Wagenknecht DR: Anti-phosphatidylethanolamine (aPE) antibodies: a survey. J Autoimmun 15: 185-193, 2000.
17) Boffa MC, Berard M, Sugi T, McIntyre JA. Kininogen reactivity of antiphosphatidylethanolamine antibodies found as the sole antiphospholipid antibodies in thrombosis and vascular cutaneous diseases. J Rheumatol, 23:1375-1379,1996.
18) Berard M, Sugi T, McIntyre JA, Chantome R, Marcelli A, Boffa MC. Prevalence and kininogen-dependence of antiphosphatidylethanolamine antibodies as sole antiphospholipid antibodies detected by ELISA. Neuv Rev Fr Hematol, 37 (Suppl II): S69-72, 1995.
19) Katsunuma J, Sugi T, Makino T. Third domain kininogen peptides are recognized by antiphosphatidylethanolamine antibodies (aPE). J Autoimmun, 15: A57, 2000 (abstract).
20) Bode W, Engh R, Musil D, Thiele U, Huber R, Karshikov A, Brzin J, Kos J, Turk V. The 2.0 A X-ray crystal structure of chicken egg white cystatin and its possible mode of interaction with cysteine proteinases. EMBO J, 7: 2593-2599, 1988.
21) Sugi T, McIntyre JA. Autoantibodies to kininogen- phosphatidylethanolamine complexes augment thrombin-induced platelet aggregation. Thromb Res, 84: 97-109, 1996.
22) Sugi T, Iwasaki K, Makino T. Spontaneous small aggregate formation (SSAF) of platelets in patients with recurrent pregnancy losses (RPL): association with antiphospholipid antibodies (aPA). J Autoimmu; 15: A72, 2000 (abstract).
23) Halbmayer WM, Mannhalter C, Feichtinger C et al: The prevalence of factor XII deficiency in 103 orally anticoagulated outpatients suffering from recurrent venous and/or arterial thromboembolism. Thromb Haemost 68: 285-290, 1992.
24) Levi M, Hack E, de Boer JP, Brandjes DPM, Buller HR, ten Cate JW. Reduction of contact activation related fibrinolytic activity in factor XII deficient patients. Further evidence of the role of the contact system in fibrinolysis in vivo. J Clin Invest 88: 1155-1160, 1991.
25) Schved JF, Dupaigne, D, Gris JC, Mares P, Neveu S. Factor XII congenital deficiency and early spontaneous abortion. Fertil Steril 52: 335-336, 1989.
26) Gallimore MJ & Winter JM: Factor XII determinations in the presence and absence of phospholipid antibodies. Thromb Haemost 79: 87-90, 1998.
27) Jones DW, Gallimore MJ, Harris S et al: Antibodies to FXII associated with lupus anticoagulant. Thromb Haemost 81: 387-390, 1999.
28) Uchida N, Sugi T, Iwasaki K, Makino T. Autoantibodies to factor XII in patients with recurrent pregnancy losses. J Reprod Immunol; 46: S25-26, 2000 (abstract).
29) Sugi T & Makino T. Autoantibodies to contact proteins in patients with recurrent pregnancy losses. J. Reprod. Immunol 53: 269-277, 2002.
30) Sugi T & Makino T. Plasma contact system, kallikrein-kinin system and antiphospholipid-protein antibodies in thrombosis and pregnancy. J Reprod Immunol 47: 169-184, 2000.
31) Margolis J. Activation of plasma by contact with glass: Evidence for a common reaction which releases plasma kinin and initiates coagulation. J Physiol 144: 1-22, 1958.
32) Kaplan AP, Josep, K, Shibayama Y, Reddigari S, Ghebrehiwet B, Silverberg M. The intrinsic coagulation/kinin-forming cascade: Assembly in plasma and cell surfaces in inflammation. Adv Immunol 66: 225-272, 1997.
33) Pettinger MA, Young R. Endotoxin-induced kinin (bradykinin) fromation: Activation of Hageman factor and plasma kallikrein in human plasma. Life Sci 9: 313-322, 1970.
34) Morrison DC, Cochrane CG. Direct evidence for Hageman factor (factor XII) activation by bacterial lipopolysaccharides (endotoxins). J Exp Med 140: 797-811, 1974.
35) Roeise O, Bouma B, Stadaas JO, Aasen AO. Dose dependence of endotoxin-induced activation of the plasma contact system: An in vitro study. Circ Shock 26: 419-430, 1988.
36) Adam A, Damas J, Galay G, Bourdon V. Quantification of rat T-kininogen using immunological methods. Biochem Pharmacol 38: 1569-75, 1989.
37) Hossain AM, Whitman GF, Khan I. Kininogen present in rat reproductive tissues is apparently synthesized by the liver, not by the reproductive system. Am J Obstet Gynecol 173: 830-4,1995.
38) Weerasinghe KM, Gadsby JE. The presence of glandular kallikrein in rabbit fetal placental conditioned medium. Endocrinology 131: 1777-1781, 1992.
39) Miatello RM, Lama M, Gonzalez S, Damiani T, Nolly H. Biochemical evidence for a kallikrein-like activity in rat reproductive tissue. Hypertension 23 (Suppl 1): 193-197, 1994.
40) Hermann A, Buchinger P, Somlev B, Rehbock J. High and low molecular weight kininogen and plasma prekallikrein/plasma kallikrein in villous capillaries of human term placenta. Placenta 17: 223-230, 1996.
41) Mutoh S, Kobayashi M, Hirata J, Ithoh N, Maki M, Komatsu Y, Yoshida A, Sasa H, Kuroda K, Kikuchi Y, Ngata I, Ohno Y. Studies on blood coagulation-fibrinolysis system regarding kallikrein-kinin system in the utero-placental circulation during normal pregnancy, labor and puerperium. Agents and Actions 38/II: 320-329, 1992.
42) Sugi T, Makino T. Antiphospholipid antibodies and kininogens in pathologic pregnancies: a review. Am J Reprod Immunol 47: 283-288, 2002.
43) Sugi T, McIntyre JA. Certain autoantibodies to phosphatidylethanolamine (aPE) recognize factor XI and prekallikrein independently or in addition to the kininogens. J Autoimmun, 17: 207-214, 2001.
|
 |
2010.05.22 Saturday
 |
|
産婦人科における抗リン資質抗体症候群
【参考文献】 『産婦人科の実際』 52巻 731-739 (2003.6)
知っておきたい生殖と免疫の知識 ─基礎から臨床までを理解するために─
8. 抗リン脂質抗体症候群
東海大学医学部母子生育学系産婦人科学部門
杉 俊隆、牧野恒久
※誠に勝手ながら文中の図1〜4につきましては掲載を省略させて頂いております。
--------------------------------------------------------------------------------
要旨
抗リン脂質抗体は、後天的血栓性素因の中でも最も重要なものの一つとして位置付けられるようになった。さらに、習慣流産、原因不明子宮内胎児死亡、子宮内胎児発育遅延、重症妊娠中毒症などとの関連も指摘されており、産科領域でも重要な位置を占めている。最近では、低用量アスピリン療法とヘパリン療法の併用が第一選択の治療として定着しており、診断がつけば適切な管理により予防可能である。本稿では、抗リン脂質抗体症候群の基礎、診断、治療について概説する。
抗リン脂質抗体とは
抗リン脂質抗体とはリン脂質に対する自己抗体であり、具体的にはカルジオリピン(CL)、フォスファチジルセリン(PS)など電気的陰性のリン脂質や、フォスファチジルエタノールアミン(PE)、フォスファチジルコリン(PC)など電気的中性のリン脂質に対する抗体である(表1)。
歴史的には、抗リン脂質抗体は梅毒血清反応陽性として検出されてきた。梅毒血清反応の測定系では、抗原としてCLとレシチン(フォスファチジルコリン)を混合したリン脂質が使用されており、したがって陽性とはCLやPCに対する抗体の存在を示している。PCに対する抗体は稀なので、一般的に梅毒血清反応陽性とは、抗CL抗体陽性ととらえられている。これは、梅毒患者が抗CL抗体陽性になる事を利用した検査法である。梅毒ではないのに抗CL抗体をもつ患者の場合、梅毒血清反応の生物学的偽陽性として抗リン脂質抗体が検出された訳である。
抗リン脂質抗体は歴史的に梅毒反応偽陽性として発見されたため、抗CL抗体が最も有名である。しかし、実際には細胞膜リン脂質の構成成分にCLは存在しない(図1)。cardio(心臓の)-lipin(脂質)という名前の通りCLは心臓に豊富に存在し、有核細胞ではミトコンドリアの内側にのみ存在する。細胞膜の構成成分としての陰性荷電リン脂質は、PSとファオスファチジルイノシトールであるが、比較的少ない。むしろ中性荷電リン脂質が主要な細胞膜の構成成分であり、PEやPC、スフィンゴミエリン(SM)がある(図1)1)。
近年、抗リン脂質抗体と不育症、血栓症との関係は広く知られており、注目を浴びている。抗リン脂質抗体は特に、後天的な血栓傾向の原因としては、最も重要なものの一つであると位置付けられるようになった2)-8)。
抗リン脂質抗体と一言で言っても、その実体は実は以前考えられていたほど単純ではない。従来は名前どおりリン脂質を認識する抗体であると思われてきたが、最近、病原性のある抗体の多くは、実はリン脂質そのものを認識する抗体ではなく、リン脂質に結合する血漿蛋白に対する抗体であるということが分かってきた。一番最初に発見された抗原はβ2-glycoprotein I(β2GPI)であり、当初はコファクターと称されたが、その後は事実上の抗CL抗体の目標抗原ということでコンセンサスが得られている。次いで、プロトロンビンが報告された。これらは、CLやPSなど、電気的陰性のリン脂質に対する抗体の対応抗原である5)。
その後我々は、中性のリン脂質であるPEに対する抗体も同様にリン脂質結合蛋白を認識することを発見し、それがキニノーゲンであることを同定した5),9)-12)。したがって、厳密にいえばこれらの抗体を抗リン脂質抗体と呼ぶのは誤りであり、それぞれ抗β2GPI抗体、抗プロトロンビン抗体、抗キニノーゲン抗体などと呼ぶべきである。しかしながら、歴史的に抗リン脂質抗体と呼ばれていたために、現在もそのままになっている13)。
抗CL抗体をELISA法で検出する際に、免疫グロブリンの非特異的結合を抑制するためにウシ血清を加えるのが一般的であるが、このウシ血清中にβ2GPIを始めとしたリン脂質結合蛋白が含まれており、抗CL抗体を検出したつもりでも、実際はCLに結合したβ2GPIを認識する抗体を検出していたわけである。しかしながら、多くの所謂"抗カルジオリピン抗体"はβ2GPIが単独で存在した場合は認識せず、CLに結合して立体構造の変化をおこして抗原性の変化したβ2GPIしか認識しないことから、"抗CL抗体"の検出には依然としてCLの存在が必須であるために、β2GPI抗体とは改名されずに今日に至っているわけである。ちなみに、梅毒患者のもつ抗CL抗体はCLそのものを認識する抗体であり、血栓症などの病原性は報告されていない。この様な、本当の抗CL抗体はβ2GPI非依存性抗CL抗体と呼ばれ、β2GPIを認識する抗CL抗体(β2GPI依存性抗CL抗体)と区別しているのが現状である。
我々が報告した、キニノーゲンを認識する抗PE抗体の場合も同様であり、抗PE抗体はCL、PS、PCなど、他のリン脂質と結合したキニノーゲンや、フリーのキニノーゲンを認識しないが、PEに結合したキニノーゲンだけを認識する14)(図2)。したがって、単純に抗キニノーゲン抗体と呼べず、キニノーゲン依存性抗PE抗体と呼んでいるのが現状である。
このように、抗リン脂質抗体といっても実は全く異なる血漿蛋白を認識する抗体の総称であり、共通点はリン脂質に結合する蛋白を認識するということだけである。したがって、それぞれの病原性は認識するリン脂質結合蛋白によって異なると考えられる。
表1 リン脂質の種類
電気的陰性のリン脂質
カルジオリピン
フォスファチジルセリン
フォスファチジルグリセロール
フォスファチジルイノシトール
フォスファチジン酸
電気的中性のリン脂質
フォスファチジルエタノールアミン
フォスファチジルコリン
抗リン脂質抗体症候群
以前よりSLEをはじめとする自己免疫疾患の患者にpregnancy lossが多いことが知られ、母体の免疫能の異常が妊娠維持に障害を起こす可能性が指摘されてきた。最近になって、それが抗リン脂質抗体という自己抗体によって惹き起こされるという説が注目されるようになり、抗リン脂質抗体と関連するpregnancy loss、血栓症をまとめて抗リン脂質抗体症候群と称し、広く認知されるようになった。抗リン脂質抗体症候群は、関連する全身疾患をもたないprimary抗リン脂質抗体症候群と、SLEやその他の膠原病を伴うsecondary抗リン脂質抗体症候群に分けられる。
表2は抗リン脂質抗体症候群診断基準案を示したものである15)。ここで注意が必要なのはpreliminary criteria(診断基準案)という表現が常に用いられていることであり、definite criteria(診断基準)ではない点である。これは本症候群が依然として曖昧であることを示しており、2年に一度開催される国際抗リン脂質抗体シンポジウムにおいてワークショップが開かれ、診断基準について話し合われている。表に示したものは、1998年に札幌で開催されたワークショップでまとめられた診断基準案である。今後は現在の診断基準案に含まれているβ2GPI依存性抗CL抗体IgG・IgMとループスアンチコアグラント(LA)以外に、抗PE抗体や抗β2GPI抗体などが考慮されるものと予想される。
表2 抗リン脂質抗体症候群診断基準案(1998;札幌Criteria)
臨床所見
血栓症: 1回またはそれ以上の
・動脈血栓
・静脈血栓
・小血管の血栓症(組織、臓器を問わない)
妊娠の異常:
・3回以上の連続した原因不明の10週未満の流産(解剖学的、遺伝的、内分泌学的原因を除く)
・1回以上の胎児形態異常のない10週以上の原因不明子宮内胎児死亡
・1回以上の新生児形態異常のない34週以下の重症妊娠中毒症または重症胎盤機能不全に関連した早産
検査所見
抗カルジオリピン抗体
・IgGまたはIgM
・中、高抗体価
・6週間以上の間隔をあけて、2回以上陽性
・β2-glycoprotein I 依存性抗カルジオリピン抗体を検出し得る標準化されたELISAで測定
ループスアンチコアグラント
・6週間以上の間隔をあけて、2回以上陽性
・International Society on Thrombosis and Hemostasisのガイドラインに従って検出
臨床所見が1つ以上、検査所見が1つ以上存在した場合、抗リン脂質抗体症候群と診断する
抗PE抗体
抗CL抗体やLAに特徴的なのは、妊娠中期以降の子宮内胎児死亡である。しかしながら、臨床で一番多く見られるのは妊娠初期流産を繰り返す不育症であり、そのような患者に対して抗CL抗体やLAを検査しても陽性にでることは期待するほどは多くない。我々は、妊娠10週未満の流産を繰り返す反復初期流産患者139人に対して、抗リン脂質抗体のスクリーニングを施行したところ、陰性荷電リン脂質を認識する抗CL抗体、抗PS抗体、LAに関しては、患者群と正常対照群で陽性率に差を認めなかったが、抗PE抗体はIgGが20.1%、IgMが12.2%、IgAが1.4%の陽性率であり、正常対照群と比較して統計学的に有意(p=0.0002)であった16)。したがって、反復初期流産患者にもっとも多く見られる抗リン脂質抗体は抗PE抗体であるという結論に達した。この事は我々が1999年に発表し、2000年になってフランスのGrisらによって同様の結果が報告された17)。さらに、不育症患者の持つPE結合蛋白依存性抗PE抗体の90.5%はキニノーゲンを認識する事が明らかになった16)。また、抗PE抗体と流産だけでなく、抗PE抗体と血栓症との関係も報告されている18-22)。
さらに抗PE抗体がキニノーゲンのどの部位を認識しているのか、合成ペプチドを用いてepitope mappingを行ったところ、約70%の抗PE抗体は、キニノーゲン、ドメイン3のLeu331-Met357 (LDC 27)を認識する事が明らかになった23)。さらに、LDC27を2つに分け、Cys333-Lys345 (CNA13)とIle346-Met357 (IYP12)を用いて検討したところ、Cys333-Lys345 (CNA13)のみを認識した23)。
LDC27 LDCNAEVYVVPWEKKIYPTVNCQPLGM
CNA13 CNAEVYVVPWEKK
IYP12 IYPTVNCQPLGM
この部位は、cystein proteinase inhibitorであるキニノーゲンが血小板上のcystein proteinaseであるcalpainに結合し、血小板活性化を抑制している部位と一致する(図3)24)。従って、抗PE抗体が結合することによりcalpainに結合できなくなり、キニノーゲンのcystein proteinase inhibitor活性が阻害されると考えられ、抗PE抗体のカリクレイン-キニン系を介した病原性を強く示唆している。
さらに我々は、抗PE抗体がキニノーゲンを認識する事により、その血小板活性化を抑制する作用を阻害し、血栓の原因となり得るかに関して、in vitroの検討を行った。キニノーゲンを認識する抗PE抗体IgGと、対照としてキニノーゲンを認識しない抗PE抗体IgGをresting 血小板に加え、トロンビンで刺激したところ、キニノーゲンを認識する抗PE抗体IgGを加えた血小板に著明な血小板凝集能の亢進が観察された(図4)25)。
抗リン脂質抗体の測定法
抗リン脂質抗体の測定はその方法から分類すると、血液凝固能検査より測定されるLAとELISA法に分けられる。LAはin vitroの血液凝固時間の延長として捉えられる。しかしながら、LAはin vivoでは出血傾向ではなく、血栓傾向を示す。長い間標準的なLAのスクリーニング法はaPTTであったが、改良されて最近では希釈Russell viper venom time (dRVVT)やKaolin clotting time(KCT)なども行われている。しかしながら、LAとして検出される抗リン脂質抗体もその対応抗原によって種類があり、これらの各測定方法は、それぞれ異なる抗原(すなわちβ2GPIやプロトロンビン)を認識するLAを検出するという報告もあり、偽陰性をなくすためには複数の方法を併用するのが望ましい。また、確認試験としては過剰のリン脂質を加えることによって中和されるかどうかを確かめる。以上のように、LAの測定系は新鮮な血漿を用いて凝固時間を測定するので、より生理的状態に近い測定法と言え、これによって見い出された抗体はかなりの信頼性で血液凝固系に影響を与え得るといえるが、感度が悪い事や、血清では測定出来ないなどの問題もある。そこで、ELISA法が開発された。ELISA法は感度も良く、精製したリン脂質やリン脂質結合蛋白を使用することにより、より特異的な抗体のみを測定することも可能である。例えば、抗CL抗体なども、ELISAの系に精製またはリコンビナントのβ2GPIを加える事により、β2GPI依存性の抗CL抗体のみを測定することが可能である。
現在当院で測定している抗リン脂質抗体は14種類である(表3)。この中で保険が適応されるのはMBL社の抗CL抗体IgG (Mesacup)とdRVVT (LA-screen, LA-confirm)、ヤマサ社の抗CL-β2GPI複合体抗体IgGのみである。MBL社のMesacupはβ2GPI以外のCL結合蛋白を認識する抗体も検出し得るので、スクリーニングには適している。しかしながら、抗CL抗体のなかでも病原性の指摘されているのはβ2GPIを認識するものであり、それを確認するのはヤマサのキットが適している。これらのキットに共通する大きな欠点は、IgGしか測定出来ないことである。IgM、IgAの陽性率は無視できず、これらを測定しないということは多くの偽陰性を生む事になる。自費にはなるが、最低IgMの測定は必須と思われる。
血栓症や妊娠中後期子宮内胎児死亡のリスクが一番高いのは、抗CL-β2GPI複合体抗体とdRVVTで測定したLAが両者とも陽性の場合であると言われている。一般病院で我々と同様の多種類の抗リン脂質抗体のスクリーニングをするのは不可能であるので、最低この2種類の測定は押さえたいものである。
妊娠初期流産を繰り返すタイプの不育症患者は、オーソドックスな抗CL抗体やLAが陽性の事は少なく、むしろ抗PE抗体を持つ事が多い16)17)。したがって、この抗体の測定も重要である。抗PE抗体IgG, IgMは現在SRL社に特殊検査として依頼すれば測定が可能である。
流産、子宮内胎児死亡以外にも抗リン脂質抗体のスクリーニングを考慮すべき疾患は表4に示した通りである。これらに該当する症例は、抗リン脂質抗体症候群の可能性を念頭において管理する必要がある。
表3 当院で測定している抗リン脂質抗体
梅毒血清反応
抗カルジオリピン抗体 IgG (Mesacup; MBL)
抗カルジオリピン-β2GPI複合体抗体IgG (Yamasa)
β2GPI依存性
β2GPI非依存性
dRVVT (LA-screen, LA-confirm; MBL)
抗フォスファチジルエタノールアミン (PE)抗体
PE結合蛋白依存性 IgG
PE結合蛋白依存性 IgM
PE結合蛋白依存性 IgA
PE結合蛋白非依存性 IgG
PE結合蛋白非依存性 IgM
PE結合蛋白非依存性 IgA
抗フォスファチジルセリン抗体
IgG
IgM
IgA
表4 産科患者において抗リン脂質抗体の存在を疑うべき状況
反復流産
原因不明妊娠中、後期の子宮内胎児死亡
早期発症、重篤な妊娠中毒症
妊娠に関連した血栓症
子宮内胎児発育遅延
自己免疫疾患または膠原病
梅毒血清反応の生物学的偽陽性
aPTTの延長
自己抗体陽性
抗CL抗体またはLAの治療
未だ不明な点の多い症候群であり、治療方針も確立してはいないが、治療の奏功率は約70-80%と報告されている。特にヘパリンが有効であり、スタンダードな治療法になりつつある26)。
最初の抗リン脂質抗体の治療法はステロイドによる免疫抑制療法であった。大量のプレドニンが必要であるが、有効性が報告されている。ヘパリン療法に匹敵するプレドニンの量は40mg/日であり、妊娠成功率は約75%と報告されている。しかしながら、プレドニンはヘパリンと比べて早産、低出生体重児、妊娠中毒症、妊娠糖尿病など副作用が多いので注意が必要である。プレドニンはヘパリンと比較して有用性に差は無いものの副作用が多いので、最近では世界的にSLEなどを合併したsecondary抗リン脂質抗体症候群の症例を除き、使用されなくなった27)。特にプレドニンとヘパリンを同時に使用すると、各々単独で使った場合に比べて有益性に差が無いにもかかわらず骨粗鬆症による骨折の危険が劇的に高まるので、併用するべきではない。
抗リン脂質抗体陽性患者における妊娠中の低用量アスピリン単独療法の役割は依然として不明である。確かにその抗血小板作用は動脈血栓を予防するかもしれないが、妊娠中における低用量アスピリン療法が不育症に対して臨床的に有効かというデータはほとんど無い。Kuttehの報告によると28)、アスピリン単独療法を受けた不育症群の生児獲得率は44%であったのに対し、ヘパリンとアスピリンの併用療法群では80%であった。この報告には無治療対照群が無いため、44%という数字が効果ありと言えるかは不明である。しかしながら、アスピリンは患者と胎児に比較的危険がないので依然として広く処方されているのが現実である。アスピリンを妊娠中に投与する場合は、妊娠初期より81mg/日を開始し、妊娠中を通して35週頃まで投与するのが一般的である。分娩時まで投与するというプロトコールもあるが、胎児動脈管早期閉鎖の危険性も考慮する必要があるので我々は35週で中止している。しかしながら、今のところそのような報告は無いので、杞憂にすぎないのかもしれない。
ヘパリン療法の有効性は多く報告されており、抗リン脂質抗体症候群の不育症の治療としてはスタンダードになりつつある。いくつかの信頼性の高い研究によると、ヘパリンと低用量アスピリン併用療法は妊娠成功率を約50%から80%に向上させると報告されている28,29)。また、最近は低分子ヘパリンの使用例も多く報告され、海外では低分子ヘパリンがスタンダードな治療法になりつつある。最近になって、妊娠中の低分子ヘパリンの安全性が綜説としてまとめられたが30)、何故か日本では低分子ヘパリンの妊娠中の投与は禁忌であり、世界の流れに逆行した決定に首をかしげざるを得ない。また、最近ヘパラン硫酸を主成分とするオルガラン(日本オルガノン)という製剤が血栓症やDICに使用され有用性が報告されている。しかしながら、ヘパラン硫酸はヘパリンとは異なるグリコサミノグリカンであり、抗リン脂質抗体症候群に有効であるというエビデンスはまだ無いので、注意が必要である。
ヘパリンが何故不育症に有効なのかは未だ不明な点も多いが、抗凝固活性以下の用量で有効な事から、その抗凝固作用よりは、陰性荷電を介して抗リン脂質抗体を吸着するなど別の作用機序も示唆されている31)。ヘパリンの投与方法としては、多くの海外の報告が5000単位を12時間毎に皮下注となっている。現在日本では皮下注用のヘパリン製剤は日本シェーリング社のカプロシンだけであるが、カプロシン皮下注用は20000単位/0.8mlであるので、1回わずか0.2mlですむ。ヘパリン投与開始時期は妊娠反応で妊娠確認出来次第であるが、過去の流産歴が妊娠6週以降の場合はまず低用量アスピリン療法を行い、超音波検査で子宮外妊娠を否定した後、ヘパリンを開始するべきと言う意見もある。ヘパリンは妊娠を通して投与し、分娩の1日前には中止する。もし緊急帝王切開など、ヘパリン投与中に分娩の必要がある場合、硫酸プロタミン(ヘパリン1000単位に対し2.5mg)を希釈して10分以上かけて静注し、中和する(50mgを超えてはならない)ことが可能である。ヘパリンの副作用としては骨粗鬆症が重要である。平均して骨密度は妊娠を通して3.7%失われると言われている32)。ヘパリン投与量が15000単位/日を超した場合は炭酸カルシウム1.5g/日を投与するべきである。ヘパリンのもう一つの重要な副作用はヘパリン惹起性血小板減少症であるが、その頻度は1%未満であると報告されている。ヘパリン投与開始後約3週間は、頻回に血小板数を測定するべきである。
抗PE抗体の治療
抗PE抗体の治療に関しては、現在試行錯誤の段階である。最近の我々の治療成績では、低用量アスピリン単独療法では妊娠成功率は75.5%、アスピリン+ヘパリン併用療法では81.1%であり、両群に差を認めなかった。しかしながら、抗PE抗体陽性不育症患者の約40%に第12因子活性低下を認め、それらの患者の妊娠成功率は、低用量アスピリン単独療法では64.7%、アスピリン+ヘパリン併用療法では92.9%であり、後者の方が成功率が高く統計学的に有意であった。
抗PE抗体のみが陽性の不育症患者の場合でも、IgGとIgMの間に治療成績の差があるのか、また、抗体価が高い場合でも低用量アスピリン単独療法で充分なのかなどに関しては、統計処理するには症例数が少なく、今後の検討課題である。個人的な経験としては、抗PE抗体IgMが陽性の場合は、抗体価が低くても病原性が強い様な印象がある。
おわりに
日本では、皮下注射用のヘパリンが病院に採用になっていないという理由で未だにプレドニンと低用量アスピリン併用療法が選択されることが多い様である。しかも、プレドニンの副作用を考え、中途半端な用量のプレドニンが投与されている事が多い。Evidence Based Medicineに基づき、可及的速やかな対応が求められる。
文献
1) Bevers EM, Comfurius P, Zwaal RFA: Changes in membrane phospholipid distribution during platelet activation. Bioch Biophy Acta, 736:57-66, 1983.
2) McNeil HP, Chesterman CN, Krilis SA: Immunology and clinical importance of antiphospholipid antibodies. Adv Immunol, 49: 193-280, 1991.
3) Hughes GRV, Harris EN, Gharavi AE: The anticardiolipin syndrome. J Rheumatol, 13: 486-89, 1986.
4) Love PE, Santoro SA: Antiphospholipid antibodies: anticardiolipin and the lupus anticoagulant in systemic lupus erythematosus (SLE) and in non-SLE disorders. Ann Intern Med, 112: 682-98, 1990.
5) Roubey RAS: Autoantibodies to phospholipid-binding plasma proteins: A new view of lupus anticoagulant and other "antiphospholipid" autoantibodies. Blood, 84: 2854-67, 1994.
6) Branch DW, Scott JR, Kochenour NK, Hershgold E: Obstetric complications associated with the lupus anticoagulant. N Engl J Med, 313: 1322-6, 1985.
7) Petri M: Pathogenesis and treatment of the antiphospholipid antibody syndrome. Advances in Rheumatology, 81: 151-177, 1997.
8) Katano K, Aoki K, Sasa H, Ogasawara M, Matsuura E, Yagami Y: b2-Glycoprotein I-dependent anticardiolipin antibodies as a predictor of adverse pregnancy outcomes in healthy pregnant women. Hum Reprod, 11: 509-12, 1996.
9) Sugi T and McIntyre JA: Autoantibodies to phosphatidylethanolamine (PE) recognize a kininogen-PE complex.Blood, 86:3083-9,1995
10) Sugi T and Makino T: Plasma contact system, Kallikrein-kinin system and antiphospholipid-protein antibodies in thrombosis and pregnancy. J Reprod Immunol, 47: 169-184, 2000
11) Sugi T, Makino T: Autoantibodies to contact proteins in patients with recurrent pregnancy losses. J Reprod Immunol, ;53:269-277, 2002
12) Sugi T, Makino T: Antiphospholipid antibodies and kininogens in pathologic pregnancies: a review. Am J Reprod Immunol, 47: 283-288, 2002.
13) McIntyre JA, Wagenknecht DR, Sugi T: Phspholipid binding plasma protein required for antiphospholipid antibody detection-an overview. Am J Reprod Immuol, 37:101-110, 1997
14) Sugi T and McIntyre JA. Phosphatidylethanolamine induces specific conformational changes in the kininogens recognizable by antiphosphatidylethanolamine antibodies. Thromb Haemost, 76:354-60,1996.
15) Wilson WA, Gharavi AE, Koike T, et al: International consensus statement on preliminary classification criteria for definite antiphospholipid syndrome. Arthritis Rheum, 42:1309-11, 1999.
16) Sugi T et al: Prevalence and heterogeneity of antiphosphatidylethanolamine antibodies in patients with recurrent early pregnancy losses. Fertil Steril, 71: 1060-5,1999.
17) Gris JC et al: Antiphospholipid and antiprotein syndromes in non-thrombotic, non-autoimmune women with unexplained recurrent primary early loss. Thromb Haemost, 84: 228-36, 2000.
18) Sanmarco M, Alessi MC, Harle JR, Sapin C, Aillaud MF, Gentile S, Juhan-Vague I, Weiller PJ: Antibodies to phosphatidylethanolamine as the only antiphospholipid antibodies found in patients with unexplained thromboses. Thromb Haemost, 85: 800-805, 2001.
19) Balada E, Ordi-Ros J, Paredes F, Villarreal J, Mauri M, Vilardell-Tarres M: Antiphosphatidylethanolamine antibodies contribute to the diagnosis of antiphospholipid syndrome in patients with systemic lupus erythematosus. Scand J Rheumatol 30: 235-41, 2001.
20) McIntyre JA & Wagenknecht DR: Anti-phosphatidylethanolamine (aPE) antibodies: a survey. J Autoimmun, 15: 185-193, 2000.
21) Boffa MC, Berard M, Sugi T, McIntyre JA: Kininogen reactivity of antiphosphatidylethanolamine antibodies found as the sole antiphospholipid antibodies in thrombosis and vascular cutaneous diseases. J Rheumatol, 23:1375-1379,1996.
22) Berard M, Sugi T, McIntyre JA, Chantome R, Marcelli A, Boffa MC: Prevalence and kininogen-dependence of antiphosphatidylethanolamine antibodies as sole antiphospholipid antibodies detected by ELISA. Neuv Rev Fr Hematol, 37 (Suppl II): S69-72, 1995.
23) Katsunuma J, Sugi T, et al: Kininogen domain 3 contains regions recognized by antiphosphatidylethanolamine antibodies. J Thromb Haemost, 2003 (in press)
24) Bode W, Engh R, Musil D, Thiele U, Huber R, Karshikov A, Brzin J, Kos J, Turk V: The 2.0 A X-ray crystal structure of chicken egg white cystatin and its possible mode of interaction with cysteine proteinases. EMBO J, 7: 2593-2599, 1988.
25) Sugi T, McIntyre JA: Autoantibodies to kininogen- phosphatidylethanolamine complexes augment thrombin-induced platelet aggregation. Thromb Res, 84: 97-109, 1996.
26) Rai R: Obstetric management antiphospholipid syndrome. J Autoimmunity, 15:203-207, 2000.
27) Silver RK et al: Comparative trial of prednisone plus aspirin versus aspirin alone in the treatment of anticardiolipin antibody-positive obstetric patients. Am J Obstet Gynecol, 169:1411-7, 1993
28) Kutteh WH: Antiphospholipid antibody-associated recurrent pregnancy loss: treatment with heparin and low-dose aspirin is superior to low-dose aspirin alone. Am J Obstet Gynecol, 174:1584-9, 1996.
29) Rai R, Cohen H, Dave M, Regan L: Randomised controlled trial of aspirin and aspirin plus heparin in pregnant women with recurrent miscarriage associated with phospholipid antibodies (or antiphospholipid antibodies). BMJ, 314:253-257, 1997.
30) Sanson BJ et al: Safety of low-molecular-weight heparin in pregnancy: a systematic review. Thromb Haemost, 81: 668-72, 1999.
31) McIntyre JA et al: Heparin and pregnancy in women with a history repeated miscarriages. Haemostasis, 23(suppl 1):202-11, 1993.
32) Mackos M, Rai R, Thomas E, Murphy M, Dore C, Regan L: Bone density changes in pregnant women treated with heparin: a prospective, longitudinal study. Hum Reprod, 14:2876-2880, 1999.
|
 |
2010.05.22 Saturday
 |
|
不育症とその治療
【参考文献】
産婦人科治療(永井書店) Vol.74 No.4 (1997:4)
牧野恒久 杉 俊隆 「不育症とその治療」
注) 赤字の部分は私が加筆したものです。
--------------------------------------------------------------------------------
はじめに
1回の独立した初期流産の頻度は統計上約15%であり、その約60%は胎児に染色体異常があると報告されている。当然患者の年齢が上がれば流産の頻度も増加する。このように自然流産の頻度はかなり多いが、3回以上流産を繰り返した場合は自然淘汰という考えでは確率的に説明できず、習慣流産という病名をつけて検索することになる。また、臨床的に妊娠と診断されない超早期流産の存在を考えると、不妊症と不育症の境界は不明であり、体外受精を繰り返しても妊娠に至らない症例なども、不育症の可能性を考慮しながら対処していく必要がある。習慣流産の原因は多岐にわたっており、系統立てた検査を施行し(表1)、総合的に判断して方針を決定する必要がある。
表1 不育症一般検査
1.問診、基礎体温
2.感染症検査
クラミジアDNA、子宮頚部・膣内培養
血算、血沈、CRP
3.内分泌検査
下垂体機能(プロラクチン)
黄体機能(黄体ホルモン、子宮内膜組織検査)
甲状腺機能(freeT3, freeT4, TSH)
糖尿病検査(空腹時血糖)
4.子宮形態異常
子宮卵管造影
5.夫婦染色体検査
6.免疫学的検査
抗核抗体、抗DNA抗体、RF
抗リン脂質抗体、Lupus anticoagulant
不規則抗体検査
7.血液凝固系検査
血小板凝集能、aPTT、TAT
1.感染
血液検査で炎症の兆候がないかを検索するとともに、クラミジア頚管炎および子宮頚部・膣内培養(目標菌GBS)を施行する。妊娠への直接的関係を調べるためには子宮頚部から直接検体を採取することをすすめる。陽性にでればそれぞれに対応する抗生剤で治療する。
2.甲状腺機能異常
甲状腺機能異常の患者に初期流産が多いことは以前より知られていたが、われわれの統計では習慣流産患者の約5%に機能異常が認められる。甲状腺機能低下症は二次的に高プロラクチン血症を引き起こすため、高プロラクチン血症を介した機序も考えられる。治療としては、機能亢進症に対してはmercazoleやPTU、機能低下症に対してはtyradin Sなどである。PTUとtyradin Sには胎盤通過性はない。mercazoleに関しては、胎盤通過性はあるものの、最近の報告ではヒトでの催奇形成に関して有意な差はないといわれている。
3. 高プロラクチン血症
習慣流産の患者の約15%に認められる。潜在性高プロラクチン血症も考慮して、疑わしい場合はTRHtestも考慮する。TRHtestでは、不可後15分でプロラクチン値70ng/ml以上を陽性とする。甲状腺機能との関連が強いので妊娠中も含めて両者を見ながら治療することが望ましい。下垂体腺腫が存在する場合は脳外科に依頼する。治療としてはパーロデルやテルロンの投与を行う。また、当然向精神薬などの副作用による高プロラクチン血症は最初に否定しておく。
4.黄体機能不全
高温期の中間でプロゲステロン値が10ng/ml未満なら治療の対象となる。黄体ホルモン経口または経膣投与やhCG筋注にて補充する。
5.糖尿病
空腹時血糖値が高い場合は75gGTTを行う。妊娠初期にコントロールできていないと胎児奇形を引き起こすので、コントロールがついてから妊娠を許可する。実際の習慣流産患者での糖尿病の頻度は低い。
6.子宮形態異常
子宮卵管造影にて子宮奇形、子宮筋腫、Asherman症候群などの有無をみる。子宮の内腔の形態が重要なのでバルーン法ではなく、し管を用いて造影することが望ましい。異常と思われる陰影が得られたときは、必要に応じて子宮鏡検査を施行する。また中隔子宮と双角子宮の識別は子宮内腔の検査では困難なの、超音波断層法、MRIや腹腔鏡にて子宮の外形を観察し、診断する。個々の形態異常の程度にもよるが、一般的に中隔子宮の流産率が最も高く、単角、双角、重複、弓状子宮等がそれに続く。子宮奇形の治療としては手術であり、Strassmann, Jones&Jones, Tompkins などの開腹手術やresectoscopeを用いた経膣手術が行なわれる。(子宮形成術を行なった場合、出産は帝王切開となる。)
7.染色体異常
女性側の染色体異常における理論的流産率はロバートソン転座で4/6(67%)、相互転座で2/4(50%)である。モザイクはその比率によって流産率は異なる。男性側の異常は受精前に淘汰されるため、最大10%程度といわれている。いうまでもなく治療は不可能であるので、理論的な流産率などに基づいたカウンセリングを行う。
8.免疫血液凝固異常
SLE(全身性エリテマトーデス)患者に流産、早産、子宮内胎児死亡などが多いことから、自己免疫疾患と妊娠予後の関連が1960年代より注目されている。また習慣流産患者の自己抗体陽性頻度は20〜30%と高率であることが判明し、自己抗体と習慣流産の関連も注目されている。妊婦スクリーニング調査によれば、妊婦の抗核抗体陽性率は10〜15%であり、決して低くない。このうち自己免疫疾患患者は1〜2%であった。したがって抗核抗体が陽性にでただけで安易に流産の原因と決めつけ治療することは慎まなければならない。しかしながら抗核抗体は習慣流産群で約20%、抗リン脂質抗体陽性の習慣流産群で約30%陽性であり、自己免疫を介する流産の一つの指標になる。
近年抗リン脂質抗体と反復流産、反復血栓症との関係が注目されている。一般的には抗カルジオリピン抗体やLupus anticoagulantのスクリーニングが行われる。これらの病原性についてはまだ不明の点も多いが、血小板凝集能亢進、血管内皮細胞活性化、血液凝固系活性化などが報告されている。注意すべきことはひとことで抗リン脂質抗体といっても、その種類は多様で、リン脂質そのものを認識する抗体や、リン脂質に結合する蛋白を認識する抗体などがあり、それぞれの目標抗原によってまったく異なる性質を持つ。たとえばリン脂質そのものを認識する抗体は知られている限りでは病原性はない。また、今までは主に電気的陰性のリン脂質に対する抗体が注目されていたが、実際にはrestingな状態では血小板や血管内皮細胞の細胞膜外皮上には陰性リン脂質は存在せず、phosphatidylethanolamine(フォスファチジルエタノールアミン:PE)などの中性のリン脂質がほとんどを占める。したがって抗PE抗体の存在を無視することはできない。われわれは抗PE抗体の多くがPEに結合するキニノーゲンを認識することを発見した。その抗体は習慣流産群や血栓症群で高率に認められ、in vitro(試験管内では)トロンビンによる血小板凝集能を亢進させることが確認された。 (東海大では学内倫理委員会の承認のもと、抗PE抗体のスクリーニング検査を研究室にて実施している。私もこの検査のために3ccの血液を提供することに同意し、検査を受けた。)
この他にも多くの未知の抗リン脂質抗体が存在することは容易に想像される。以下に、免疫血液凝固系検査の結果をいくつかのパターンに分けて、治療方針をまとめる。
1.抗リン脂質抗体症候群
抗リン脂質抗体の陽性(Lupus anticoagulamtも含む)の治療法に関してはまだ確立していない。抗リン脂質抗体の目標抗原によって血栓形成機序が異なるために、治療法もケースバイケースであると思われる。現時点での主な治療法は、低用量アスピリン療法、ヘパリン、プレドニン、柴苓湯などがある。低用量アスピリン療法は、アスピリン81mg/日を妊娠初期より投与し、分娩の1週間前には中止する。血小板凝集能を抑制する作用は81mg/日で十分であり、より強い効果を期待して増量することは出血などの副作用を招くだけで無意味である。ヘパリン療法は、妊娠初期よりヘパリン10,000単位/日投与する。トロンビン増加例(TAT上昇、prothrombin fragment1+2上昇、AT3減少)で効果が期待できる。胎盤通過性がないので、胎児に対しては安全である。プレドニン療法は、抗リン脂質抗体の抗体価を低下させることを期待する治療である。投与量は抗体価による。副作用を考え、特に妊娠中は慎重に投与すべきである。柴苓湯はプレドニン作用と、血小板凝集能抑制作用を持つと報告されている。妊娠中通して投与する。
2.抗核抗体のみ陽性
反復流産の既往があり、抗リン脂質抗体は陰性で抗核抗体のみ陽性にでることは、よくある。抗核抗体は免疫系のアンバランスの指標にはなるが、抗核抗体自体の病原性は報告されておらず、安易に抗リン脂質抗体症候群に準じた治療を行うことは慎むべきである。しかしながら、これらの患者さんは未知の抗リン脂質抗体を持っている可能性は否定できない。原因不明のIUGR(子宮内発育遅延)や子宮内胎児死亡などの既往がある場合は注意が必要である。また血小板凝集能が亢進している場合は低用量アスピリン療法を、TATやprothrombin fragment 1+2高値の場合は低用量アスピリン療法やヘパリン療法を考慮すべきである。
3.自己抗体、血液凝固検査すべて正常
3回以上の流産歴がある原因不明習慣流産患者の場合は、夫リンパ球による免疫療法を考慮する。流産歴2回の場合は、免疫療法は予後を改善しないというデータが複数の施設より報告されており、副作用も考慮すると免疫療法の適応とならない。もちろん流産歴2回の場合は、本当に何も流産の原因がないということが多いと思われる。免疫療法はその作用機序についていくつかの報告があるが、不明の点も多い。副作用については感染症、GVHD(移植片対宿主病)、不規則抗体の出現などがある。GVHDは放射線照射によって防止できる。不規則抗体については、新たな不妊症、流産の原因をつくりだす可能性がある。また、胎児に作用して胎児水腫を引き起こす可能性もある。このように免疫療法は作用機序が不明なうえに安全性が確立されている訳でもないので,慎重に考慮し、十分なインフォームドコンセントが必要である。
|
 |
2010.05.22 Saturday
 |
|
流産と自然淘汰
1回目の稽留流産を医師から告げられた時、このような説明がありました。
「流産は全妊娠のおよそ15%に起こると言われていて、決して珍しいことではありません。今回は胎児に何らかの染色体異常があった可能性が高いですね。残念ではありますが、自然淘汰とお考えください。」はじめて聞く話に、その時は医師の話を十分理解することができませんでした。
同じような経験をされた方は意外と多いのではないでしょうか?というわけで、あらためて「流産と自然淘汰」についてまとめてみようと思います。
報告する施設によって多少のばらつきはあるものの、一般的に妊娠の
約15%は自然流産に終わると言われています。厚生省心身障害研究班報告(平成3〜5年度)によると、自然流産の頻度は14.9%、うち妊娠12週未満の早期流産は13.3%、妊娠12週以降22週未満の後期流産は1.6%とされており、流産が妊娠初期に起こりやすいことは明らかなようです。
初期流産の最大の原因は胎児(胎芽)の染色体異常でその確率は約60〜70%とも言われています。すなわち、このような胎児の染色体異常による流産は自然淘汰を意味するということです。尚、このような胎児染色体異常による流産に予防法はないとされています。
PlachotとOharaらの説によれば(図1参照)、卵子の染色体異常が26%、
精子の染色体異常が8%、そして受精過程での染色体異常が8%とされ、受精時には約40%もの染色体異常があると計算されています。そして、その15%は卵割期に、さらに15%が着床前後に淘汰され、10%が妊娠と診断された後に流産というかたちで淘汰されます。このように卵割期、着床前後といった我々の無意識の過程においても、染色体異常における自然淘汰は起こっているわけです。この染色体異常の発生率は加齢とともに増加するということですから、高齢になるほど流産率は増加することになります(表1参照)。初期流産を経験された方のなかには、流産の原因は自分にあると思いこまれ、自分自身を責めていらっしゃる方も多いやに感じています。そのような方に是非この「流産の基本的考え方」について知ってもらい、少し冷静になって流産を受け止めてもらえたらと思います。
但し、このような流産が度重なるとなると話は違ってきます。流産の頻度を約15%とすると、連続2回流産となるのは2.3%、流産を3回繰り返すのはは0.34%と計算されます。したがって、2回までの流産であれば偶然が重なっただけという可能性もありますが(私の場合はこの段階で不育症の検査を受けました)、流産を連続して3回以上繰り返した場合は単なる偶然では説明できないので、そこに何らかの原因があると考え、「習慣流産」として原因を検索することが必要となります。
図1.染色体異常妊卵の発生と出生前淘汰
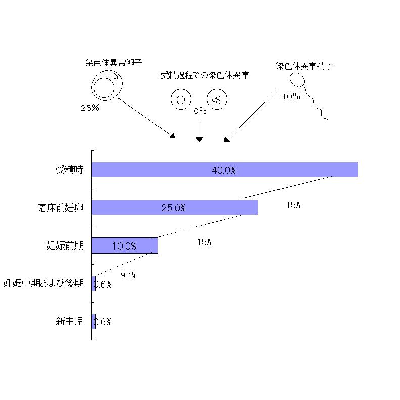
表1.母体年齢別にみた流産歴および妊卵の染色体異常率
大濱紘三
母体年齢 流産率(%) 妊娠に占める胎児
染色体異常(%)
〜29 30〜34 35〜39
40〜 15 17〜18
25〜30 4〜5 5〜6
10 20〜25
図1ならびに表1の参考文献
・牧野恒久, 和泉俊一郎, 杉俊隆 : 総論 不育症. 新女性医学体系15 不妊・不育 (中山書店)
・Plachot M, Veiga A, Montagut J, et al : Are clinical and biological IVF parameterscorrelated with chromosomal disorders in early life : a multicentric study. Hum Reprod 1988 ; 3 : 627-635
・大濱紘三 : 妊娠早期流産に関する新しい考え方. 日医医報 1992 ; No.505 : 10-11
|
 |
2010.05.22 Saturday
 |
|
GOOD NEWS です。
東海大学付属伊勢原病院の研究室でしか測定できなかった抗PE抗体が
東海大以外の病院でも測定可能となりました。
SRLという全国ネットの検査会社が1999年6月から
検査受付を開始しています。
SRLは全国ネットの検査会社で、
ほとんどの総合病院が検査を依託しているそうなので、
事実上、国内の多くの病院で抗PE抗体が測定可能となったと言えるか
と思います。
ちなみに抗PE抗体の正常値はキニノーゲン依存性、非依存性とも
0.3未満です。
これはまさに全国の不育症患者にとって朗報ですね。
特に、現時点で「原因不明」と診断されている方、
「リンパ球移植」に臨まれる前に、
一度主治医にお問合せなさっては如何でしょうか?
ちなみに検査費用ですが、保険適応外とのことで、
5,000円程度と聞いています。
私が東海大で検査を受けた際は無料だったので、
今回あらためて確認したところ、
不育外来に通院する患者さんについては、従来通り研究室で検査を行い、
陽性と出た人のフォローアップに関してはSRLに依頼する予定とのこと。
費用については引き続き無料とのことです。(1999年7月9日現在)
抗PE抗体とは・・・
抗リン脂質抗体のひとつであり、電気的中性のリン脂質、
フォスファチジルエタノールアミン(PE)に対する抗体である。
このPEに対する抗体もPEそのものを認識せず、
PEに結合する血漿蛋白である
キニノーゲンを認識する。PEは常に血管内皮細胞や血小板などの
細胞膜外層に存在し、その主要成分であることから、
抗PE抗体が血栓を惹き起こす可能性は十分にある。
また抗PE抗体IgGが試験管内でrestingな血小板の
トロンビン惹起性血小板凝集能を亢進させることが報告されている。
【参考文献】
産婦人科の世界 Vol.49 杉 俊隆 牧野恒久
「習慣流産抗リン脂質抗体陽性例の検査、治療」
|
 |
2010.05.22 Saturday
 |
|
産科外来④ 1999.11.20〜
1999.11.20 34w3d
尿検査、超音波検査、NST、ドップラー → 特に異常なし。順調とのことです。
浮腫 → またもや+
最後のカプロシン処方

毎度ながら腕です。

これは難解。目と目と鼻。上から見た絵です。
残念ながら今回は2枚しか頂けなかった・・・
1999.11.30 35w6d
尿検査、NST、ドップラー、内診 → 異常なし。
浮腫 → マイナス(^。^)
おりもの検査、血液検査
カプロシン&バファリン中断。
1999.12. 7 36w6d
尿検査、NST、ドップラー → 異常なし
浮腫 → ± (^_^;)
おりもの検査、血液検査 → 特に異常なし。貧血もOK!
1999.12.14 37w6d
尿検査、NST、ドップラー → 特に異常なし
浮腫 → マイナス(^.^)(^.^)
内診
1999.12.21 38w6d
尿検査、NST、ドップラー → 異常なし
浮腫 → かろうじてマイナス(^_^;)
内診 → 依然として子宮口に変化なし
血液検査
1999.12.28 39w6d
尿検査、NST、ドップラー → 異常なし
浮腫 → マイナス
内診 → かろうじて一指分開いているらしい(^_^;)
12/21の血液検査 → 特に異常なし
2000. 1. 5 41w0d 陣痛を誘発するため入院
9:30 NST、剃毛
15:30 子宮口を柔らかくする注射
16:20 ドップラー
18:30 内診→子宮口の開きは未だ一指→ラミナリア挿入
23:00 陣痛室へ
NST→胎児心拍に異変→ラミナリア摘出、子宮収縮を抑える注射
2000. 1. 6 41w1d
1:00 胸部レントゲン、心電図、抗生剤チェック
1:16 帝王切開開始
2:00 オペ終了(卵巣嚢腫も合わせて摘出)
1:42 2598g の女児誕生
詳細については出産報告を・・・
2000. 1.13 内診、抜糸
2000. 1.15 母子ともに無事退院
2000. 2. 8 産後1ヶ月検診
尿検査、内診 → 異常なし
|
 |
2010.05.22 Saturday
 |
|
産科外来③ 1999.9.5〜
1999. 9. 5 23w3d
尿検査、超音波検査、ドップラー →特に異常なし。順調とのこと。
血液検査
カプロシン、小児用バファリン、鉄剤処方。

頭部断面画像

顔を斜めからみた画像

手、ひじ、腕の部分

足の裏
1999. 9.19 25w3d
尿検査、ドップラー→特に異常なし
9月5日の血液検査→12因子活性127% 貧血やや改善するも未だ基準値以下
浮腫±→塩分摂取注意要
カプロシン、鉄剤処方。
1999. 9.28 26w6d
尿検査、超音波検査、ドップラー→特に異常なし
超音波検査によると、どうやら女の子らしい・・・
血液検査
カプロシン、小児用バファリン、鉄剤処方。

左:眼球と鼻を上から見たところらしい
右:腕部(だいぶたくましくなってきた)

左:顔を斜め上からみたところ。見ようによっては非常にリアル。
右:???よくわかりません
1999.10.16 29w3d
尿検査、ドップラー→特に異常なし
血色素10.5g/dl→やや改善す基準値以下→鉄剤処方
カプロシン処方
1999.10.27 31w0d
尿検査、超音波検査、ドップラー→特に異常なし
血液検査
浮腫+→塩分制限
小児用バファリン、カプロシン、鉄剤処方

顔の側面に手腕部をのっけてるところ

恒例!足の裏。随分大きくなった。

横顔

左:お鼻のアップ(鼻の穴がバッチリ)
右:顔
(共に画像は横向き)
1999.11. 7 32w3d
尿検査、NST※、ドップラー → 特に異常なし
浮腫±、貧血ようやく基準値まで改善。
カプロシン処方。(鉄剤はパスです!)
※NSTとは・・・
妊娠9ヶ月からこの検査が加わります。
検査室の張り紙を読むと、ノン・ストレス・テストの略ということで、赤ちゃんがお産のストレスに耐えられるかを調べる検査ということです。どうやら赤ちゃんの心拍や運動状況、母体の子宮収縮をモニターしいるようでした。実査時間は15分程度。
インターネットで調べてみたら・・・
「赤ちゃんの健康状態をチェックするための検査。また、赤ちゃんが産道を通って無事に生まれてくるだけの元気があるかどうかを見る検査。胎動があったとき赤ちゃんの心拍数が増えれば元気な証拠!心拍数に変わりがないときは、赤ちゃんには自然分娩に耐えるだけの力がない!!ということに・・・」ということでした。ナルホド!
|
 |
2010.05.22 Saturday
 |
|
産科外来② 1999.7.3〜
1999. 7. 3 14w3d
経腹エコー検査→順調とのことです。
内診、ドップラーにて心音確認。
尿検査、血液検査、カプロシンならびに小児用バファリン処方

全体像です。大きさは?です。

右のバーコードみたいなものは、胎児の心臓の動きをモニターしているそうです。
下にある156bpmは胎児の心拍数かな?

胎児の頭を俯瞰から見たものです。大横径30mmということ?

これは胎児の手腕部分です。
1999. 7.17 16w3d
ドップラーにて心音確認。内診→特に異常なし
7/3の検査結果:血液凝固12因子活性88%
カプロシン処方
1999. 8. 4 19w0d
尿検査、超音波検査、内診、ドップラー →異常なし
血液検査、カプロシン処方
午後から母親学級に出席

胎児の横顔

胎児の頭

胎児の手腕。何かをゆび指してるみたいです。

足の裏。足を交差させているみたいです。
1999. 8.21 21w3d
尿検査、ドップラーにて心音確認。→特に異常なし
カプロシン処方
【8/4の血液検査の結果】
12因子活性52%
貧血(血色素9.5g/dl)→鉄剤(フェロミア錠50mg)処方
|
 |
2010.05.22 Saturday
 |
|
産科外来① 1999.4.26〜
1999/4/19
生理周期27日に少量の出血があるが、その後の出血がほとんど見られず*、基礎体温も高温が続いていることから、高温期から服用している小児用バファリンは継続。
* 着床時に見られる「月経様出血」というものらしい。
1999/4/21
市販の妊娠判定薬で検査してみたところ、陽性反応が出る。
1999/4/22
「月経様出血」とは違うと思われる出血(どす黒い血塊)が少量あり。
1999/4/23
排泄時に茶色いオリモノ有。24日も同様に続く。
1999/4/25
22日と同様の出血有。茶色いオリモノも続く。
小児用バファリン服用により出血しやすくなるという認識はあったが、あらためて「切迫流産」の危険性を感じる。
1999/4/26(4w5d)
切迫流産とヘパリン治療**のため緊急入院。
経膣エコーで胎嚢3.3mm確認。子宮外妊娠を否定。
血液検査。午後からヘパリンの24時間点滴開始。(5000単位/日)
**私自身の血液凝固12因子の活性低下の原因として、12因子を認識する抗体陽性の可能性が出てきたことから、主治医とのインフォームド・コンセントのもと、急遽小児用バファリンとヘパリンを併用することに決定。東海大の場合、ヘパリン治療の方法として24時間の点滴もしくは12時間ごとの皮下注射がある。私の場合、働いていることもあり長期入院は不可能なため、早速ヘパリンの自己注射の練習をすることになる。
1999/5/1(5w3d)
経膣エコーで胎嚢12.7mm確認。12因子活性(26日実施分)・・・57%
血液検査・尿検査。

1999/5/2
茶色いおりもの止まる。
1999/5/5(6w0d)
食間のむかつき出てくる。
1999/5/6(6w1d)
経膣エコーにて心拍確認。
自己注射開始。12時間おきにヘパリン(カプロシン)0.1mlを大腿部に皮下注射する。

ほとんど原寸大です。案外小さい注射器でしょ?
1999/5/8
出血もおさまり、心拍も確認。自己注射もおぼえて晴れて退院。
1999/ 5/15(7w3d)
産科外来へ
経膣エコーにて胎芽12mm、並びに心拍確認。
尿検査、血液検査、カプロシン処方。

1999/5/20(8w1d)
経膣エコーにて胎児19mm、心拍確認。
血液検査、カプロシン処方。

1999/5/29(9w3d)
経膣エコーにて胎児29mm、少し動いていました。
5.15の血液検査結果・・・12因子50%
尿検査、カプロシン処方。

1999/6/6(10w3d)
経膣エコーにて36.7mmの胎児確認。手足を動かしていました。
血液検査。バファリン、カプロシン処方。

1999/6/15(11W6d)
経膣エコー、胎児の頭殿長57mm。
6/6の血液検査の結果、血液凝固12因子活性・・・72%
尿検査、血液検査。カプロシン処方。

1999/6/19(12W3d)
経膣エコー、胎児の頭殿長64mm。超音波ドップラーで心音を確認。
カプロシン処方。

|
 |
2010.05.22 Saturday
 |
|
不育外来② 2001.1.24〜
検査&治療の経過 part2
--------------------------------------------------------------------------------
2001/1/24
血液検査
前回異常値を示した項目(抗リン脂質抗体、血液凝固12因子、プロラクチン)について再検査実施。
2月某日
1/24の検査の結果、やはり12因子は33%と妊娠前の数値に見事にもどっており、次の妊娠もヘパリン+アスピリンの併用療法となる予定。プロラクチンに関しては、ありがたや、正常値に戻っていたため、テルロンの服用はなし。テルロンとの相性は最悪なので助かりました。一応、バファリンを処方してもらう。

|
 |
2010.05.22 Saturday
 |
|
不育外来① 1998.11.4〜
1.検査内容
(1) 問診、基礎体温
(2) 感染症検査
クラミジアDNA、子宮頚部・膣内培養、血算、血沈、CRP
(3) 内分泌検査
下垂体機能(プロラクチン)
黄体機能(黄体ホルモン)
甲状腺機能(freeT3, freeT4, TSH)
糖尿病検査(空腹時血糖)
(4) 子宮形態異常
子宮卵管造影
(5) 免疫学的検査schedule.htm
抗核抗体、抗DNA抗体、RF(リウマトイド因子)
抗リン脂質抗体(抗PE抗体含む)、Lupus anticoagulant
不規則抗体検査
(6) 血液凝固系検査
血小板凝集能、aPTT、TAT、血液凝固第12因子
2.検査・治療の経過
注)以下に紹介する内容は、あくまでもひとつの症例であり、決して一般論化されるべきものではないことを、はじめにお断り致します。
1998/11/4 初診
問診、基礎体温の確認
子宮頚部検体採取 → 感染症検査
血液検査→免疫学的検査
1998/11/19
血液検査→内分泌検査
1998/11/26
血小板凝集能検査→血液凝固系検査
1998/11/30
子宮卵管造影検査(し管法)→子宮形態検査
1998/12/3
血液再検査(黄体ホルモン、血液凝固第12因子)
【それまでの検査結果】
プロラクチン・・・25.9ng/ml→高プロラクチン血症
テルロン錠0.5を1錠/日を処方される
黄体ホルモン・・・8.7ng/ml→再検査
血液凝固第12因子活性値・・・44.7%→再検査
他は特に異常なし。
1998/12/17
【12. 3の再検査結果】
黄体ホルモン・・・14.7ng/ml→異常なし
1999/1/13
【12.3の再検査結果】
血液凝固第12因子活性値・・・50%→小児用バファリン1錠/日を処方される
注)現在までのところ、12因子と流産との関連は証明されているわけではありません。よって治療法に関しても研究段階にあります。小児用バファリンについては、主治医とのインフォームド・コンセントのもとに服用しています。詳しくは12因子に関する最近の論文を参照ください。血液凝固第12因子と習慣流産について
1999/2/17
血液再検査(プロラクチン)
経膣超音波検査(卵巣に皮様嚢腫あり。定期的に検査しています。約3×3cm、変化なし)
卵巣腫瘍マーカー
1999/3/17
血液再検査(血液凝固12因子、抗カルジオリピン抗体*)
*1回目の検査で、リン脂質結合蛋白ではなく、リン脂質そのものを認識するβ2GPI非依存性の抗カルジオリピン抗体が検出されましたが、現在までのところ、その抗体の病原性は認められておらず,反復流産との関連も不明と聞いています。
【2.17の再検査結果】
プロラクチン・・・2.3ng/ml→テルロン服用中止
1999/4/14
【3.17の再検査の結果】
血液凝固12因子活性値・・・42%
→高温期スタート日から次の生理まで小児用バファリンを1日1錠服用。妊娠の場合は、出産4週前まで服用を続けることになります。
抗カルジオリピン抗体(β2GPI非依存性)・・・3.1U/ml
| chezsmile | 不育外来 | 17:01 | - | - |
|
 |
|

|
































